(1)下图所示是实验室中制取气体的一种简易装置。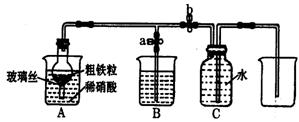
①甲同学用下列方法检验装置的气密性,请问能否达到目的 (填能或否)
关闭止水夹a和b,从A处烧杯中加入水,使干燥管与烧杯中液面形成液面差,一段时间后,液面差没有变化,说明气密性良好。
②实验室利用上图所示发生装置可以制取下列 气体。
| A.Cl2 | B.CO2 | C.H2S | D.SO2 |
(2)乙同学利用该图所示装置,用粗铁粒与3mol·L-1硝酸反应制取NO气体。请回答有关问题。
①NO气体能用排水法收集,而不能用排空气法收集的可能原因是 。
②制取NO时,向A杯中加入稀硝酸,同时打开止水夹a,关闭止水夹b,A装置的干燥管中观察到气体的颜色的变化为 。B装置烧杯中液体的作用是 。当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体。
③将a mol铁与含b molHNO3的稀溶液充分反应后,若HNO3的还原产物只有NO,反应后Fe和HNO3均无剩余,则反应中转移电子的物质的量为 mol(用含b的代数式表示)。
(1)有四种物质是:①0.5molCO2 ②6gH2 ③1.204×1024个HCl ④147gH2SO4,它们中物质的量最大的是 ,所含分子数最多的是 ,含有原子数最多的是 ,质量最大的是_ (用序号填空)。
(2)配制100 mL浓度为1 mol·L-1的稀硫酸,需要用98%密度为1.84 g/cm3的浓硫酸 mL。
根据题目要求书写化学用语:
(1)碳酸氢钠的电离方程式 。
(2)钠和水反应的离子方程式 。
(3)符合CO2+2OH—===CO32-+H2O的化学方程式 。
(4)请配平如下的化学方程式:
K2Cr2O7+ HCl ═ KCl+ CrCl3+ Cl2↑+ H2O
浓盐酸在上述反应中体现的性质有
| A.还原性 | B.氧化性 | C.酸性 | D.既有氧化性又有还原性 |
某无色溶液中含有CO32-、K+、NH4+、Ba2+、SO42-、Fe3+中几种离子,今取二份体积各100mL该溶液进行实验。
(1)第一份加入足量氢氧化钠浓溶液,加热,产生的氨气在标准状况下体积为896mL;
(2)第二份加入足量氯化钡溶液,生成沉淀质量为6.27g,再经足量稀盐酸洗涤后得2.33g残渣。
据此回答:
①用稀盐酸洗涤沉淀时反应的离子方程式为 ;
②含有的阴离子及其对应物质的量浓度依次是 ;
③对是否存在K+的判断依据是 。
向烧杯中加25mL蒸馏水,加热至沸腾,立即滴加6滴饱和FeCl3溶液,继续煮沸至溶液呈透明红褐色。冷却后将其净化既成功制得介稳体系R。试回答:
(1)R中分散质直径为 ;
(2)煮沸时反应的离子方程式为 ;
(3)判断该实验成功的实验方法是(填名称) ;
(4)向R中逐滴加入稀硫酸至过量,实验现象是 ,最后得到棕黄色溶液。
海藻中含有丰富的KI。实验室从海藻灰中提取I2的流程如下:①海藻灰溶于水制成悬浊液→②经操作A得到KI溶液→③通入Cl2反应得到含I2水溶液→④经操作B得到含碘苯溶液→⑤I2晶体试回答:
(1)操作A实验名称是 ;
(2)操作B中,除夹持仪器外,还需要烧杯和 (填仪器名称);
(3)步骤③中反应的离子方程式为 。