NA表示阿伏加德罗常数,下列说法正确的是( )
①标准状况下,11.2 L SO3所含有的原子数目为2NA
②3.4 g氨中含有0.6NA个N—H键
③36.5 g HCl气体中含有Cl―数为NA
④1.2g NaHSO4晶体中阳离子和阴离子的总数为0.03 NA
⑤室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA
⑥12.4g白磷晶体中含有的P-P键数是0.6NA
⑦1.5 g CH3+中含有的电子数为NA
⑧常温下,100 mL1 mol·L-1AlCl3溶液中阳离子总数小于0.1NA
⑨78 gNa2O2晶体中所含阴阳离子个数均为2NA
⑩2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2NA
| A.④⑥⑨⑩ | B.②⑤⑥⑩ | C.①③④⑥ | D.③⑦⑧⑨ |
图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线错误的是()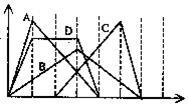
| A.向NaAlO2溶液中滴入HCl至过量 |
| B.向澄清石灰水中通入CO2至过量 |
| C.向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量 |
| D.向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至沉淀消失 |
某课外活动小组的同学从采集器中获得粉尘颗粒样品,然后用蒸馏水溶解,得到可溶性成分的浸取液。在探究该浸取液成分的实验中,下列根据实验现象得出的结论错误的是()
| A.取浸取液少许,滴入AgNO3溶液有白色沉淀产生,则可能含有Cl- |
| B.取浸取液少许,加入Cu和浓H2SO4,试管口有红棕色气体产生,则可能含有NO3- |
| C.取浸取液少许,滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,则一定含SO42- |
| D.用洁净的铂丝棒蘸取浸取液,在酒精灯外焰上灼烧,焰色呈黄色,则一定含有Na+ |
如图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨能还原氧化铁):a. Al; b.Fe2O3; c.NaOH溶液; d. HI溶液;e.NH3;f.Cl2 。图中⑤表示的物质是()
| A.a或b | B.c | C.d | D.e或f |
在2L密闭容器内,按物质的量之比为2︰1投入NO和O2。某温度下发生如下反应:
2NO(g) + O2(g) 2NO2(g),n(NO)随时间的变化如表:
2NO2(g),n(NO)随时间的变化如表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.020 |
0.015 |
0.012 |
0.010 |
0.010 |
0.010 |
下列说法不正确的是
A.在0~2s内,v(O2)=0.002mol·L-1·s-1
B.5s后向容器中通入0.02mol NO2,再次平衡后,0.020mol<n(NO2)<0.040 mol
C.在该温度时,向容器中加入O2,平衡将正向移动,平衡常数增大
D.5s后,向反应容器中同时通入各0.01mol的NO、O2、NO2,平衡向正向移动
下列溶液中微粒的物质的量浓度关系一定正确的是
| A.0.1 mol·L-1NH4Cl溶液与0.05 mol·L-1NaOH溶液等体积混合后所得的碱性溶液中: c(Cl-)>c(NH4+)>c(Na+)>c(H+)>c(OH-) |
| B.等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+) |
| D.某二元弱酸的酸式盐NaHA溶液:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) |