在常温下,某水溶液M中。
(1)若M中存在的离子只有:Na+、CH3COO-、H+、OH-,下列关系合理的是 。
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+) ②c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
③c(H+)>c(OH-)>c(Na+)>c(CH3COO-) ④c(Na+)=c(CH3COO-)且c(OH-)=c(H+)
(2)若M由两种相同物质的量浓度的溶液混合而成,其中只存在OH—、H+、NH4+、Cl-四种离子,且c(NH4+)>c(Cl-)>c(OH—)>c(H+),这两种溶液的溶质是 。
(3)若M为0.01 mol/L的氨水,向其中加入等体积pH=2的盐酸溶液(忽略溶液体积变化),所得混合液中:c(NH4+)+c(H+)-c(OH-)= 。
(4)若M为20 mL稀硫酸和盐酸混合液,向该混合酸溶液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60 mL Ba(OH)2溶液时,C点溶液的pH=7(忽略溶液体积变化),试计算: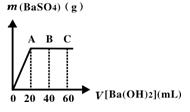
(i)最初混合酸溶液中c(H2SO4)=__________,c(HCl)=____________。
(ii)B点溶液的pH为多少?(写出计算过程。可能用到的数据:1g2=0.30、1g3=0.48)
某有机物由C、H、O三种元素组成,它的红外吸收光谱表明有羟基O—H键和烃基上 C—H键的红外吸收峰,且烃基和羟基上氢原子个数之比为2:1,它的相对分子质量为62,试写出该有机物的结构简式。
请你按官能团的不同对下列有机物进行分类: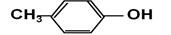

H2O由液态变为气态的过程可以用下式来表示:
H2O(l) H2O(g)。我们也可以用平衡移动原理来解释这一变化中的一些问题,如:H2O
H2O(g)。我们也可以用平衡移动原理来解释这一变化中的一些问题,如:H2O 的汽化是吸热过程,所以温度升高,平衡向生成更多的H2O(g)的方向移动。请回答下面两个问题:
的汽化是吸热过程,所以温度升高,平衡向生成更多的H2O(g)的方向移动。请回答下面两个问题:
(1)减小压强,平衡向移动。所以高山上由于空气稀薄,水的沸点比平地上
(填高或 低)。高压锅中水的沸点比普通锅中水的沸点(填高或低)。
低)。高压锅中水的沸点比普通锅中水的沸点(填高或低)。
将除去氧化膜的镁条插入到稀盐酸溶液中, 发现生成氢气的速度变化情况如下图所示:
其中t1—t2速度变化的主要原因是
t2—t3速度变化的主要原因是
己知维生素A的结构简式可写为 式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C.H原子未标记出来,维生素A中碳原子个数为个,氧原子个数为个。
式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C.H原子未标记出来,维生素A中碳原子个数为个,氧原子个数为个。