AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):  ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓
;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓 度,以 (填“促进”、“抑制”)其水解。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
度,以 (填“促进”、“抑制”)其水解。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(10分)降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产甲醇燃料。为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH =-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH =-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。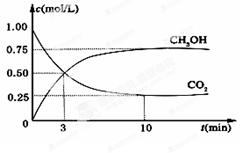
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=________mol/(L·min);
(2)氢气的转化率=________;
(3)该反应的平衡常数为________(保留小数点后2位);
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是________。
| A.升高温度 |
| B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离出去 |
| D.再充入1mol H2 |
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1________c2的关系(填“>”、“<”或“=”)。
Ⅰ、火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652KJ的热量。
(1)反应的热化学方程式为。
(2)又已知H2O(l)=H2O(g);ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是KJ。
此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是。
Ⅱ、下图表示在密闭容器中反应:2SO2+O2 2SO3, △H< 0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是;b c过程中改变的条件可能是;若增大压强时,反应速度变化情况画在c~d处.。
2SO3, △H< 0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是;b c过程中改变的条件可能是;若增大压强时,反应速度变化情况画在c~d处.。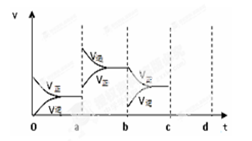
煤燃烧的反应热可通过以下两种途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+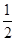 O2(g)===H2O(g)ΔH=E3③
O2(g)===H2O(g)ΔH=E3③
CO(g)+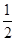 O2(g)===CO2(g)ΔH=E4④
O2(g)===CO2(g)ΔH=E4④
请回答:
(1)与途径a相比,途径b有较多的优点,即______________________________________。
(2)上述四个热化学方程式中的哪个反应ΔH>0?____________。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是_______。
A.a比b多B.a比b少C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为______________________________。
(5)已知:
①CO(g)+1/2O2(g)=CO2(g) ΔH1= -283.0 kJ/mol
②H2(g)+1/2O2(g)=H2O(l) ΔH2= -285.8 kJ/mol
③C2H5OH(l)+ 3O2(g)=2CO2(g)+3H2O(l) ΔH3="-1370" kJ/mol
则④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=______________。
(共6分)(1)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后得到密度为1.17 g·cm-3的溶液。请计算:
①混合后的溶液中NaCl的质量分数是
②混合后的溶液的物质的量浓度为mol/ L
(2)在标准状况下,1L水溶解了一定体积的NH3,所得溶液的密度为ρg·cm-3,物质的量浓度为amol·L-,则所溶解的NH3的体积为L
(8分)现有 A、B、C、D、E五瓶无色溶液分别是HC1、BaCl2、NaHSO4、K2CO3、AgNO3溶液中的一种,已知:
①A与B反应有气体产生
②B与C反应有沉淀生成
③C与D反应有沉淀生成
④D与E反应有沉淀生成
⑤A与E反应有气体产生
⑥在②、③反应中生成的沉淀为同一种物质.
请填写下列空白: (1)A是,B是,D是。
(2)写出⑤反应的离子方程式.
(3)将 0.1 mol/L 的 Ba(OH)2溶液与 0.1 mol/L 的E溶液按下表中的不同配比进行混合:
| 甲 |
乙 |
丙 |
丁 |
戊 |
|
| 0.1 mol/L 的Ba(OH)2溶液的体积/mL |
10 |
10 |
10 |
10 |
10 |
| 0.1 mol/L 的E溶液的体积/mL |
5 |
10 |
15 |
20 |
25 |
①按丁方式混合后,所得溶液显 (填"酸""碱""中" )性.
②按乙方式混合时,反应的离子方程式为.