下列不符合“节能减排”要求的做法是
| A.将煤液化、气化,提高燃料的燃烧效率 |
| B.在大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃料电池汽车 |
| C.拉闸限电,减少发电厂用煤量 |
| D.研制和开发一个与植物光合作用相近的化学反应系统,是解决能源问题的研究方向之一 |
在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+ 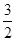 O2(g) = SO2(g)+H2O(g) △H 1
O2(g) = SO2(g)+H2O(g) △H 1
②2H2S(g)+SO2(g) = 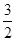 S2(g)+2H2O(g) △H 2
S2(g)+2H2O(g) △H 2
③H2S(g)+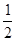 O2(g) = S(g)+H2O(g) △H 3
O2(g) = S(g)+H2O(g) △H 3
④S(g) = 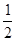 S2(g) △H4
S2(g) △H4
则△H 4的正确表达式为()
A.△H 4 =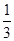 (3△H 3 - △H 1 - △H 2) (3△H 3 - △H 1 - △H 2) |
B.△H 4 =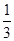 (△H 1 + △H 2 - 3△H 3) (△H 1 + △H 2 - 3△H 3) |
C.△H 4 = (△H 1 + △H 2 - 3△H 3) (△H 1 + △H 2 - 3△H 3) |
D.△H 4 = (△H 1 - △H 2 - 3△H 3) (△H 1 - △H 2 - 3△H 3) |
常温下,下列各组离子在指定溶液中一定能大量共存的是()
①0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-、NO3-
⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-、S2-
| A.①③⑤ | B.② | C.②④⑥ | D.④⑤ |
设NA为阿伏加德罗常数的值,下列各项叙述正确的是()
①1 molCl2参加反应转移电子数一定为2NA
②1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
③标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA
④1L 2mol·L-1的Al(NO3)3溶液中含Al3+个数为2NA
⑤1 L 2 mol/L的氯化铁溶液完全制成胶体,氢氧化铁胶体的粒子数小于2 NA
⑥6.0 g SiO2晶体中含有的硅氧键数目为0.4 NA
⑦1 molCH3+ 所含的电子数为8NA
⑧在标准状况下,2.8 g N2和2.8 g CO所含电子数均为1.4 NA
⑨300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA
⑩标准状况下,2.24 L乙醇分子所含的C-H键数为 0.5NA
| A.②③⑦⑧⑨⑩ | B.①②③⑤⑧⑨ | C.②⑤⑥⑦⑧ | D.②④⑦⑧⑩ |
下列选项中有关离子方程式的书写正确的是( )
| A.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| B.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C.过量的CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O=HCO3-+HClO |
| D.硫化钠水溶液呈碱性的原因:S2-+2H2O=H2S+2OH- |
下列装置、试剂选用或操作正确的是( )
| A.除去NO中的NO2 | B.用于AlCl3蒸发结晶 | C.稀释浓硫酸 | D.制备少量O2 |