下图为以惰性电极进行电解。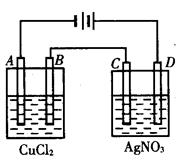
(1)写出A、B、C、D各电极上的电极方程式:
A_________________________B_______________________
C_________________________D_______________________
(2)在A、B、C、D各电极上析出生成物的物质的量比
下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。
请回答下列问题:
(1)B中所含元素位于周期表中第周期,族。
(2)A在B中燃烧的现象是。
(3) 的反应中,被氧化与被还原的物质的物质的量比是。
的反应中,被氧化与被还原的物质的物质的量比是。
(4)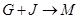 的离子方程式是。
的离子方程式是。
(5)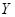 受热分解的化学方程式是。
受热分解的化学方程式是。
Ⅰ.某些化学反应可表示为:A+B→C+D+H2O。请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为____________________。
(2)若A为黑色固体,C、D均为气体,则该反应的化学方程式为________。
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色有刺激性气味的气体,若A为盐,B为酸,则A是或______(填化学式)。
(4)若A是铁的一种氧化物,B是硫酸,则A与B反应的化学方程式为____。
Ⅱ.某些化学反应可表示为:A+B +H2O→C+D。请回答下列问题:
若反应物与生成物中各有一种物质含有Si元素,请写出2个符合要求的化学反应方程式
,
(1)某研究性学习小组在实验室中配制1 mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是______________。
A、实验中所用到的滴定管、容量瓶,在使用前均需要检漏;
B、如果实验中需用60 mL 的稀硫酸标准溶液,配制时应选用100 mL容量瓶;
C、容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小;
D、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大;
E、配制溶液时,若在最后一次读数时俯视读数,则导致最后实验结果偏大。
F、中和滴定时,若在最后一次读数时俯视读数,则导致最后实验结果偏大。
(2)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-) / c(H+)=1×10-8。
①常温下,0.1 mol·L-1 HA溶液的pH=;写出该酸(HA)与NaOH溶液反应的离子方程式:;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是:;
③0.2 mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合后所得溶液中:
c(H+)+c(HA)-c(OH-)=mol·L-1。(溶液体积变化忽略不计)
(3)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw= 。
①该温度下(t℃),将100 mL 0.1 mol·L-1的稀H2SO4溶液与100 mL 0.4 mol·L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=。
②该温度下(t℃),1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是:。
已知A、B、C、D、E五种主族元素分属三个短周期,且原子序数依次增大。A、C同主族,可形成离子化合物CA;B、D同主族,可形成DB2、DB3两种分子。请回答下列问题:
(1)元素E在元素周期表中的位置是,五种元素原子半径由小到大的顺序为(用元素符号回答)。
(2)A、B两种元素能形成两种常温下呈液态的化合物M、N,具有强氧化性的化合物M的电子式可表示为;化合物N在同主族元素形成有具有相同结构的物质中,具有较高的沸点,其原因是。
(3)在上述元素最高价氧化物对应的水化物中酸性最强的是(写化学式,下同),非金属气态氢化物还原性最强的是。
(4)A、B、C、D中的三种或四种元素能形成多种离子化合物,其水溶液呈碱性的有(写出所有化合物,用化学式表示,下同),呈酸性的有(写出所有化合物)。
(5)元素B、E的单质或两元素之间形成的化合物可作水消毒剂的有(写出其中两种物质的化学式)。
烃A是一种重要的基本化工原料,用质谱法测得其相对分子质量为28。下图是以A为原料合成药物中间体E和树脂K的路线。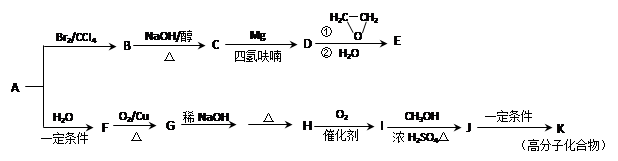
已知:I. 
II. 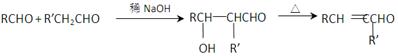
(R、R’表示烃基或氢原子)
(1)A中官能团的结构简式是。有机物B的名称
(2)B→C的化学方程式为。B和氢氧化钠的水溶液加热反应所得到的有机产物和乙二酸反应生成高分子化合物,写出生成高分子化合物反应的化学方程式
(3)E的分子式为C4H8O。下列关于E的说法正确的是(填字母序号)。
a. 能与金属钠反应b. 分子中4个碳原子一定共平面
c. 一定条件下,能与浓氢溴酸反应d. 与CH2=CHCH2OCH2CH3互为同系物
(4)G→H涉及到的反应类型有。
(5)I的分子式为C4H6O2,其结构简式为。
(6)J→K的化学方程式为。
(7)写出与E具有相同官能团的所有同分异构体的结构简式:
(不考虑顺反异构,不考虑—OH连在双键碳上的结构)。