写出下列物质在水溶液里的电离方程式:
(1)硫酸铁 ;
(2)氢氧化铝 ;
(3)硫酸氢钾 。
下面列出了几组物质,请将物质的合适组号填写在空格上。同位素,同系物,同分异构体,同素异形体。
①金刚石与“足球烯”C60;②D与T;③16O、17O和18O;
④氧气(O2)与臭氧(O3);⑤CH4和CH3CH2CH3;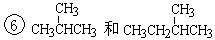 ;
;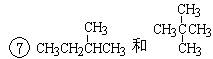
(14分)向体积为 2L 的固定密闭容器中通入3molX 气体 , 在一定温度下发生如下反应:2X (g) Y (g) +3Z (g)
Y (g) +3Z (g)
(1). 经 5min 后反应达到平衡 , 此时测得容器内的压强为起始时的 1.2 倍 , 则用 Y 表示的速率为mol/L·min。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行 , 在同一段时间内测得容器内的反应速率分别为 : 甲、 v (X) ="3." 5 mol/L·min; 乙、 v (Y) ="2" mol/L·min; 丙、 v (Z) ="4." 5 mol/L·min; 丁、 v (X) ="0." 075 mol/L·s。若其它条件相同 , 温度不同 , 则温度由高到低的顺序是 ( 填序号〉
(3) 若向达到 (1) 的平衡体系中充入惰性气体, 则平衡向( 填"左"或"右"或"不)移动;若向达到 (1) 的平衡体系中移走部分混合气体 , 则平衡向( 填 " 左 " 或 " 右 " 或 " 不 ") 移动。
(4)若在相同条件下向达到 (1) 所述的平衡体系中再充入 0.5molX 气体 , 则平衡后 X 的转化率与(1) 的平衡中的 X 的转化率相比较
| A.无法确定 | B.前者一定大于后者 | C.前者一定等于后者 | D.前者一定小于后者 |
(5)若保持温度和压强不变 , 起始时加入 X 、 Y 、 Z 物质的量分别为 amol 、 bmol 、 cmol, 达到平衡时仍与 (1) 的平衡等效 , 则 : a 、b 、c应该满足的关系为
(6)若保持温度和体积不变 , 起始时加入 X 、 Y 、 Z 物质的量分别为 amol 、 bmol 、 cmol, 达到平衡时仍与 (1) 的平衡等效 , 且起始时维持化学反应向逆反应方向进行 , 则c 的取值范围应该为
(10分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g)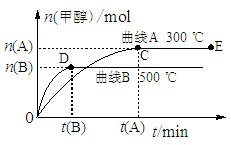
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=,升高温度,K值(填“增大”、“减小”或“不变”)。
(2)在500 ℃,从反应开始到平衡,氢气的平均反应速率v (H2)=。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加d.重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:______________________________ (用化学方程式表示)。
(16分)10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度(填“大于”或“小于”)NaHCO3。丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则(填“甲”或“乙”)判断正确。试剂X是。
| A.Ba(OH)2溶液 | B.BaCl2溶液 | C.NaOH溶液 | D.澄清的石灰水 |
(2)将加热后的溶液冷却到10℃,若溶液的pH(填“高于”、“低于”或“等于”)8.3,则
(填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言(填“甲”或“乙”)判断是错误的,理由是。
(8分)目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图。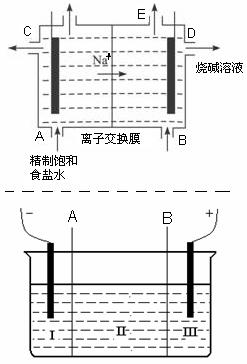
(1)下列说法不正确的是
| A.从E口逸出的气体是H2 |
| B.从B口加入含少量NaOH的水溶液以增强导电性 |
| C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH |
| D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加 Na2CO3溶液 |
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),在这种电解池中电解Na2SO4溶液可制得氢氧化钠、硫酸等物质。A为离子交换膜、B为离子交换膜(填“阴”或“阳”),电极均为惰性电极。Na2SO4溶液应该在区(填“I”、“II”、“III”)加入。通电电解时阴极的电极反应式为,在III区得到。当外电路总共通过30 mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为: