铜合金及铜的氯化物在生产生活中有着广泛的应用。请回答下列问题:
(1)向硫酸铜、氯化钠混合溶液中滴加亚硫酸钠溶液生成CuCl沉淀,实验测得溶液的pH与亚硫酸钠溶液体积的关系曲线如图所示。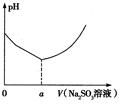
①用离子方程式解释亚硫酸钠溶液呈碱性的原因: 。
②用离子方程式解释图像中V<a时溶液酸性增强的原因: 。
当V>a时,随着亚硫酸钠溶液的体积增大,溶液pH增大的原因是 。
(2)已知:Ksp(AgCl)=8×10-10,Ksp(CuCl)=1.2×10-6。向CuCl 浊液中滴加硝酸银溶液,发生反应CuCl(s)+Ag+(aq) AgCl(s)+Cu+(aq),该反应平衡常数K= 。
AgCl(s)+Cu+(aq),该反应平衡常数K= 。
(3)硫酸铜溶液中含少量硫酸铁,加入氢氧化铜,过滤,除去三价铁离子,写出加入氢氧化铜时发生反应的离子方程式: 。
(4)测定CuCl和CuCl2混合物中CuCl含量的原理为用氯化铁溶液溶解样品,以邻菲罗啉作指示剂,用Ce(SO4)2溶液滴定至终点,滴定反应为Ce4++Fe3+=Fe2++Ce3+。氯化铁与氯化亚铜反应的离子方程式为 。
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为.
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)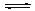 N2(g)+2CO2(g);△H<0.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K=.
N2(g)+2CO2(g);△H<0.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K=.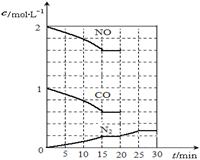
若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将移动(填“向左”、“向右”或“不”).
20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是(填序号).
①加入催化剂②降低温度
③缩小容器体积④增加CO2的量
(3)肼(N2H4)用亚硝酸氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977.写出肼与亚硝酸反应的化学方程式.
(4)如图所示装置可用于制备N2O5,则生成N2O5的那一极电极反应式为 .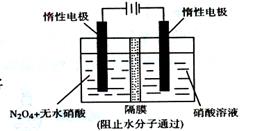
选做[化学——选修3:物质结构与性质]已知A、B、C、D、E、F都是元素周期表中前36号的元素,它们的原子序数依次增大。A的一种单质是自然界硬度最大的物质,B是地壳中含量最多的元素,C的单质能从B的一种氢化物中置换出B的一种单质,D是人体骨骼中的常见元素,D的氢氧化物常用来检验A和B形成的一种化合物,F的原子序数比E大1,F是Ⅷ族元素中原子序数最小的一种元素。
(1)E的基态原子电子排布式为,比较F和 E的各级电离能后发现,气态E2+再失去一个电子比气态F2+再失去一个电子难,其原因是。
(2)写出 DA2的电子式。
(3)DC2的一个晶胞如图所示,则图中实心球表示D还是C?
答:(填元素名称)。该晶体的密度为a g/cm3,则晶胞的体积是(只要求列出算式)。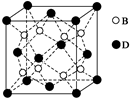
(4)AB32- 离子的空间立体构型为,AB气体在配合物中常作为配体,如近年来开始使用的一种新型汽油防震剂F(AB)5,该化合物中F元素的化合价为。
选做[化学——选修2:化学与技术](15分)生态工业园区的建设,不仅仅是体现环保理念更要依据循环经济理论和充分考虑经济的可持续发展。下图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产三大生态产业链流程图。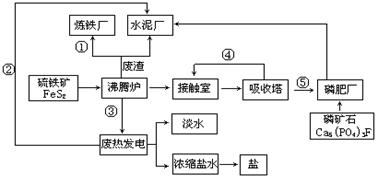
根据上述产业流程回答下列问题:
(1)从原料、能源、交通角度考虑该企业应建在。
| A.西部山区 | B.沿海地区 | C.发达城市 | D.东北内陆 |
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式
①,②,③,④,⑤。
(3)沸腾炉发生反应的化学方程式,磷肥厂的产品是普钙,其主要成份是(填化学式)。
(4)热电厂的冷却水是,该流程中浓缩盐水除提取盐以外还可提取的物质有(写出一种即可)。
(5)根据生态园区建设理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想,(请写出两点)。
钒是一种重要的合金元素,还用于催化剂和新型电池。从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如下:
部分含钒化合物在水中的溶解性如下表:
| 物质 |
V2O5 |
NH4VO3 |
VOSO4 |
(VO2)2SO4 |
| 溶解性 |
难溶 |
难溶 |
可溶 |
易溶 |
请回答下列问题:
(1)反应①所得溶液中除H+之外的阳离子有。
(2)反应②碱浸后滤出的固体主要成分是(写化学式)。
(3)反应④的离子方程式为。
(4)25℃、101 kPa时,4Al(s)+3O2(g)==2Al2O3(s)ΔH1=-a kJ/mol
4V(s)+5O2(g)==2V2O5(s)ΔH2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是。
(5)钒液流电池(如下图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为,电池充电时阳极的电极反应式是。
(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2VO+2+H2C2O4+2H+===2VO2++2CO2↑+2H2O。取25.00 mL 0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为g/L。
(14分)雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6 kJ·mol-1
2SO3(g)ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)ΔH=kJ·mol-1。
SO3(g)+NO(g)ΔH=kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有。
a.体系密度保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K=。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
(3)下图是一种用NH3脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为H2O和(填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为L。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示,写出NO分解的化学方程式。