一定条件下,在密闭容器内,SO2氧化成SO3的热化学方程式为:2SO2 (g) + O2 (g) 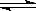 2SO3 (g);△H=-a kJ·mol-1在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可能是
2SO3 (g);△H=-a kJ·mol-1在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可能是
| A.4molSO2和2molO2 | B.5molSO2和3molO2 |
| C.4molSO2和4molO2 | D.2molSO2、1molO2和2molSO3. |
现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要时可加热)能用于鉴别它们的是
①观察颜色 ②石蕊试剂 ③品红溶液
| A.只有①② |
| B.只有①③ |
| C.只有②③ |
| D.①②③ |
下列过程最终无沉淀产生的是
| A.过量氨气通入Al2(SO4)3溶液 |
| B.CO2通入CaCl2溶液 |
| C.少量SO2通入BaCl2溶液后再通入过量Cl2 |
| D.过量CO2通入Na2SiO3溶液 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
| A.将NaHCO3固体加入新制氯水,有无色气泡(H+) |
| B.使红色布条褪色(HCl) |
| C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈血红色(Cl2) |
| D.滴加AgNO3溶液生成白色沉淀(Cl-) |
硫酸厂有一辆已存放过浓硫酸的铁槽车。某工人违反规定,边吸烟边用水冲洗,结果发生了爆炸事故。下列对引起爆炸的原因分析正确的是
| A.浓硫酸遇明火爆炸 |
| B.浓硫酸遇水发热爆炸 |
| C.铁与水(常温下)产生的氧化物爆炸 |
| D.稀释后的硫酸与铁反应产生的氢气接触空气并遇明火而爆炸 |
对于反应:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O,下列有关说法中不正确的是
| A.HNO3在反应中既表现氧化性也表现出酸性 |
| B.每生成22.4L NO(标准状况)有3mol电子转移 |
| C.HNO3作氧化剂,铜作还原剂,3molCu还原8 mol的HNO3 |
| D.HNO3作氧化剂,铜作还原剂,3molCu还原2 mol的HNO3 |