某实验小组在测定黄铜(铜和锌的合金)组成时,甲、乙、丙、丁四位同学分别取质量相等的黄铜样品与一定量的稀硫酸反应,所得数据记录如下表所示:
| 样 品 |
甲 |
乙 |
丙 |
丁 |
| 黄铜样品质量/g |
50 |
50 |
50 |
50 |
| 稀硫酸的质量/g |
20 |
40 |
60 |
80 |
| 产生气体质量/g |
0.2 |
0.4 |
0.5 |
0.5 |
试分析计算:
(1)在乙同学测得的数据中, 已反应完全(填写物质的名称)。
(2)黄铜样品中含有铜的质量分数是多少?
如图A、B、C三种物质都含有同一种元素,B是单质, A、C都是氧化物,C是一种黑色固体物质。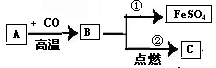
请回答:
(1)写出C的化学式;
(2)写出反应①的化学方程式;
(3)指明反应②基本反应类型。
由一种可溶性碱和两种可溶性盐组成的固体混合物A,为探究其组成,取适量混合物A进行如下实验:(假设每一步均恰好完全反应)
根据上述实验推断:
(1)蓝色沉淀是。
(2)原混合物A中一定含有的一种物质是;另外两种物质可能是和。
有一种工业废水,含有大量的ZnSO4和少量CuSO4以及污泥。兴趣小组的同学想从中回收金属铜和硫酸锌晶体,他们设计了如下方案: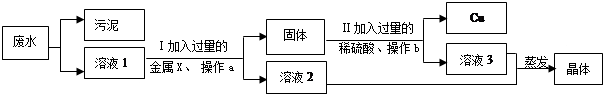
(1)操作a、b的名称是,其目的是除去溶液中。步骤Ⅱ中发生反应的化学方程式为。
(2)甲同学提出X可用金属铁,乙同学认为X可用金属锌,你认为(填“甲”或“乙”)同学的意见是正确的,理由是。步骤Ⅰ中加入过量的金属X的目的是。
(3)若溶液1和溶液2中溶质ZnSO4的质量分数分别表示为a、b,则a、b的大小关系是__________;溶液3中的溶质是(填化学式)。
金属元素在生活、生产中,以及对人类的健康有着很重要的作用,请回答下列问题。
(1)金属加工后的废切削液中含有2~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl=NH4NO2+X
第二步:NH4NO2=N2↑+2H2O
①第一步反应中X的化学式是。
②NH4NO2中氮、氢、氧三种元素的质量比是,其中氮元素的化合价分别是,。
(2)如图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验。
①小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的等发生了化学反应。
②小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为。
③我国古代将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到约800℃,得到一种外观似金子的合金,该合金的主要成分为,试写出有铜生成的化学方程式。
(3)用金属铁制备自来水的新型消毒、净水剂K2FeO4的流程如下:请回答下列问题:
①固体B的成分是,反应a的化学方程式为:。
②操作I的名称是;操作I所需要的仪器和用品:铁架台、玻璃仪器、试剂、(填一种实验物品名称)。
③反应a、b、c中没有涉及到的化学反应类型是(填字母代号)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
已知常用的酸跟常用的碱反应生成的盐的水溶液显中性。现将某蓝色晶体A溶入某一无色中性液体中,按下图所示过程进行实验: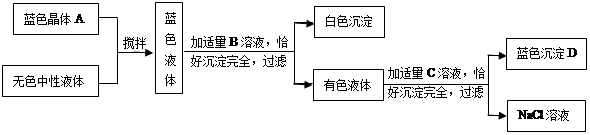
试按要求填写下列空白:
(1)写出B、C溶液中溶质的化学式:B,C ,蓝色沉淀D是。
(2)若A是纯净物,无色中性液体是只含有一种溶质的溶液,则其溶质是。
(3)写出有色液体与C溶液反应的化学方程式。