“温室效应”是哥奉哈根 世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是 (填字母编号)。
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导“低碳”生活
c.利崩太阳能、风能等新型能源替代化石燃料 ·
(2)CH4是另一种主要的温室气体,l克甲烷完全燃烧生成液态水和二氧化碳,放出55.64 kJ的热量,甲烷的燃烧热是 。
(3)酸阿的形成主要是由废气中的SOx和NOx造成的。通过SO2和Br2、H2O的定量反应在电解池中产生的电流变化,可以准确测定空气中SO2的含量。该反应的化学方程式为 ,反应中氧化产物和还原产物的物质的量之比为 。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。
第一阶段燃烧黄铁矿的化学方程式为 ;
第二阶段的反应原理是2SO2(g)+O2(g) 2SO3(g),其生产设备的名称为 ;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2SO3(g),其生产设备的名称为 ;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是 (填字母编号)
a. SO2为5mol·L-1,O2为3.5mol·L-1
b. SO2为3mol·L-1
c.SO2、SO3均为2.5mol·L-1
d.SO3为5mol·L-1
I、二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。比Cl更好。
⑴在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
用方法二制备的ClO2更适合用于饮用水消毒,其主要原因是。
⑵用ClO2处理过的饮用水(pH 5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO2—)。
饮用水中的ClO2、ClO2—含量可用连续碘量法进行测定。ClO2被I—还原为ClO2—、Cl—的转化
率与溶液pH的关系如下图所示。当pH≤2 .0时,ClO2—也能被I—完全还原为Cl—。反应生成
的I2用标准Na2S2O3溶液滴定;2Na2S2O3+ I2= Na2S4O6 + 2NaI
①请写出pH≤2 .0时ClO2—与I—反应的离子方程式。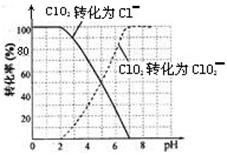
②请完成相应的实验步骤:
步骤1:准确量取V mL水样加入到锥形瓶中。
步骤2:调节水样的pH为7.0~8.0。
步骤3:加入足量的KI晶体。
步骤4:加入少量淀粉溶液,用c mol·L-1Na2S2O3
溶液滴定至终点,消耗Na2S2O3溶液V1mL。
步骤5:。
步骤6:再用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。
③根据上述分析数据,测得该饮用水中ClO2—的浓度为mol·L-1(用含字母的代数式表示)。
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差 ,工业上用湿法制备高铁酸钾的基本流程如下图所示:
,工业上用湿法制备高铁酸钾的基本流程如下图所示:
⑴在农业生产中,滤液1可用作。
⑵流程中生成高铁酸钾的离子方程式是:,控制此反应温度30℃以下的原因是: 。
。
⑶结晶过程中加入浓KOH溶液的作用是:。
⑷某温度下,将Cl2通入KOH溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是2:3,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为。
⑸实验测得铁盐溶液的质量分数、反应时间与K2FeO4产率的实验数据分别如图1、图2所示。为了获取更多的高铁酸钾,铁盐的质量分数应控制在附近、反应时间应控制在。
、能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1) 工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)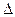 H1
H1
反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)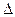 H2
H2
①上述反应符合“原子经济”原则的是(填“Ⅰ”或“Ⅱ”);
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
由表中数据判断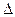 H10(填“>”“=”或“<”);
H10(填“>”“=”或“<”);
③某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为.
(2)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应Ⅰ进行甲醇合成,T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应 到某时刻测得各组分的浓度如下:
到某时刻测得各组分的浓度如下:
| 物质 |
H2 |
CO |
CH3OH |
| 浓度/(mol·L-1) |
0.2 |
0.1 |
0.4 |
①比较此时正、逆反应速率的大小:v正v逆(填“>”、“<”或“=”)。
②若加入CO、H2后,在T5℃反应10min达到平衡,c(H2)=0.4 mol·L-1,则该时间内反应速率v(CH3OH) =mol·(L·min)-1。
(3)生产过程中,合成气要进行循环,其目的是。
、下列A~K是中学化学中的常见物质,其中D、E、K为单质,其余物质为化合物。这些物质具有下列转化关系(省略了水和部分反应物及生成物),除反应②外,其他反应均在水溶液中进行。其中D是工业中最常用的金属。回答: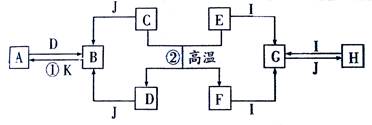
(1)A、H分别为、(填化学式)
(2)写出反应②的化学方程式。
(3) 2.7克E与I完全反应生成G,若G与J反应生成3.9克不溶物H ,则消耗J的物质的量为。
(4)若实验测得无水H在常压条件下不同温度时的密度为:
| T(℃) |
200 |
600 |
800 |
| ρ(g/L) |
6.881 |
2.650 |
1.517 |
| 气体摩尔体积(L/mol) |
38.8 |
71.6 |
88.0 |
则 600℃时无水H存在形式的分子式为。
原子序数由小到大排列的四种短周期主族元素X、Y、Z、W,其中Z、W两原子的核外电子数之和为X、Y两原子核外电子 电
电 子数之和的三倍,Y、Z左右相邻,Z、W位于同一主族。
子数之和的三倍,Y、Z左右相邻,Z、W位于同一主族。
(1)Y元素是(填元素名称)。
(2)由X、Y、Z三种元素组成的盐中存在的化学键为。
(3)解释WZ2的水溶液显酸性的原因(用方程式表示)。
(4)某物质由Na、Y、Z三种元素组成,取该物质配成的溶液,滴加AgNO3溶液,有白色沉淀生成,再滴入稀HNO3,白色沉淀溶解,该物质的分子式为。
(5)分别均由X、Y、Z、W四种元素组成的化合物A和B,它们之间能以物质的量1:1进行反应。写出A与B两溶液反应的离子方程式。
(6)Y2X4是一种可燃性的液体,其燃烧产物之一是大气中的主要成分。1 .60g Y2X4在氧气中完全燃烧放出热量31.2 kJ(25℃),请写出Y2X4完全燃烧的热化学反应方程式。
.60g Y2X4在氧气中完全燃烧放出热量31.2 kJ(25℃),请写出Y2X4完全燃烧的热化学反应方程式。
碳酸钙常用作牙膏 的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2)
的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2)
回答下列问题:
(1)充分煅烧110吨石灰石得到固体66吨,则石灰石中碳酸钙的质量分数为%。
(2)假设第①步反应完全进行,则第②步反应过滤后得到的不溶液性滤渣的成分为
。
(3)第③步反应一般不采用通入CO2的主要原因是 ,相应的离子方程式为。
,相应的离子方程式为。
(4)CaCO3是一种难溶液物质,25℃时其KSP=2.8×10-9。现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2.0×10-4mol/L,则生成沉淀所需CaCl2溶液的物质的量浓度最小是。
(5)某生用石灰石为原料,设计了另一种制备碳酸钙的实验方案,其流程图如下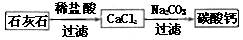
与前一方案相比较,该方案的优点是。