我国规定饮用水质量标准必须符合下列要求:
| PH |
6.5~8.5 |
| Ca2+、Mg2+总浓度 |
<0.0045mol/L |
| 细菌总数 |
<100个/mL |
某综合实践活动小组到自来水厂参观,了解到源水处理成自来水的工艺流程示意图如下: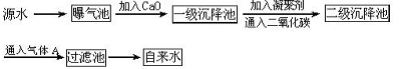
(1)源水中含有Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后发生若干个化学反应,请写出其中任意一个反应的离子方程式:_____________________________________
(2)加入絮凝剂可以除去其中的悬浮固体颗粒,该过程是____________________(填序号)
①只有物理过程,无化学过程
②只有化学过程,无物理过程
③既有物理过程,又有化学过程
(3)FeSO4·7H2O是常用的絮凝剂,加入后最终生成红褐色胶状沉淀,则这种沉淀是___________(填化学式)
(4)通入二氧化碳的目的是__________和___________。
(5)物质A的作用是_________,则A可以选择下列物质中的__________(填序号)
①ClO2 ②SO2 ③液氯 ④Ca(ClO2)2 ⑤浓硫酸
(共15分)
下列物质的相互转化关系中,甲、乙、丙是三种金属单质,甲燃烧时,火焰呈黄色;A、C、D为气体,C在通常情况下呈黄绿色;H为红褐色沉淀物(图中部分反应的条件和生成物未全部标出)。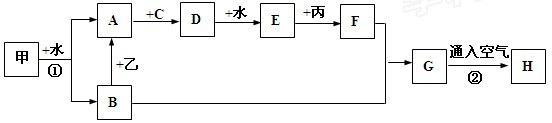
(1)B的俗名:;E的名称:。
(2)①写出反应①的离子方程式:;
②写出B→A的离子方程式:;
③写出反应②的化学方程式:;
此过程中物质的颜色变化情况为:。
(3)①写出反应C +丙反应的化学方程式:;
②写出反应C + F反应的离子方程式:。
③若C+F的产物为I,则检验I中阳离子的试剂是:(化学式),现象为。
某二元酸(化学式用H2A表示)在水中的电离方程式是(第一步电离完全):
H2A="=" H+ +HA- HA-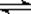 H+ + A2-
H+ + A2-
回答下列问题:
(1)Na2A溶液显____________(填“酸性”、“中性”、“碱性”)
理由是:(用离子方程式表示)__________________________________________。
(2)0.1mol/L的H2A溶液的pH_________1(填“<”“=”“>”)
(3)0.1mol/L的Na2A溶液中,下列微粒浓度关系错误的是_____________。
| A.c(Na+) =2c(A2-) =" 0.2" mol/L |
| B.c(OH-) = c(H+) + c(HA-) |
| C.c(Na+) + c(H+) = c(OH-) + c(HA-) + 2c(A2-) |
| D.c(Na+) =" 2c" (A2-) + 2c (HA-) |
可逆反应:aA(g)+ bB(g) cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答:
(1)压强 P1比P2(填大或小);(2)(a +b)比(c +d)(填大或小);
(3)温度t1℃比t2℃(填高或低);(4)正反应为反应。
t℃时,将3 mol A 和1 mol B气体,通入体积为2L的密闭容器(容积不变),发生反应:3A(g) + B(g) 4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
(1)从反应开始到达到平衡状态,生成C的平均反应速率为_______________________。
(2)达到平衡状态时,B 物质的转化率α(B) = _____________,
平衡常数K= _____________________(填计算结果)。
(3)若继续向原混和物质通入少量氦气后(设氦气不与A、B、C反应),化学平衡__________(填字母)
A、向正反应方向移动 B、向逆反应方向移动 C、平衡不移动。
(4)若向原平衡中再充入a mol C,在t℃时达到新平衡,此时B的物质的量为:
n(B) = ___________________ mol.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间该满足的关系为:
____________________________________。
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)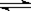 CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=。
(2)该反应为反应(选填“吸热”、“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是(多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为℃。