(共15分)
下列物质的相互转化关系中,甲、乙、丙是三种金属单质,甲燃烧时,火焰呈黄色;A、C、D为气体,C在通常情况下呈黄绿色;H为红褐色沉淀物(图中部分反应的条件和生成物未全部标出)。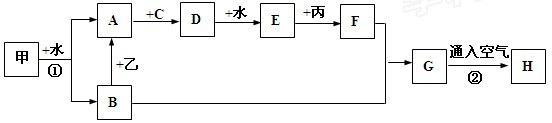
(1)B的俗名: ;E的名称: 。
(2)①写出反应①的离子方程式: ;
②写出B→A的离子方程式: ;
③写出反应②的化学方程式: ;
此过程中物质的颜色变化情况为: 。
(3)①写出反应C +丙反应的化学方程式: ;
②写出反应C + F反应的离子方程式: 。
③若C+F的产物为I,则检验I中阳离子的试剂是: (化学式),现象为 。
依据氧化还原反应:2Ag+(aq) + Cu(s) ="=" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。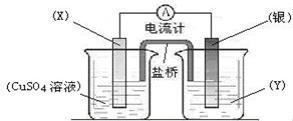
请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方程式:_____________ 。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式: FeSO4+ K2O2 → K2FeO4+ K2O+ K2SO4+ O2↑,当转移了1.5NA个电子时,在标况下可收集到 升氧气。
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,高铁酸钾作为水处理剂发挥的作用是______________________ 。
NH3在工业生产上有重要的应用
(1)写出用浓氨水检验氯气管道泄漏的化学反应方程式
(2)若将少量氨气与过量氯气混合,则生成一种酸和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式 ;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式 .
锰的化合物种类较多,也大多具有广泛的用途。
I.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性。某化学兴趣小组通过实验探究MnO2的性质。
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是_____________。
A.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把MnO2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2 SO3溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeSO4溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在
室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸。现象记录如下:
| 试管编号 |
实验现象 |
| A |
溶液不变色 |
| B |
溶液缓慢变浅棕褐色 |
| C |
溶液迅速变棕褐色 |
从以上实验中,我们可以得出的结论是____________。
②写出C试管中发生反应的离子方程式:________________。
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机。MnFe2O4的制备工艺流程如下图:
已知Fe3+、Mn2+沉淀的pH如表所示。
| 开始沉淀 |
完全沉淀 |
|
| Fe3+ |
2.7 |
4.2 |
| Mn2+ |
8.3 |
10.4 |
①步骤一中投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比理论上应为___________________。
②步骤二中需控制pH的范围是_______________
③步骤三中是否洗涤干净的判断方法是_____________.
CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益.
(1)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1=-820kJ/mol
②CO(g)+H2O(g)=CO2(g)+H2(g)△H2=-41.2kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H3=-566kJ/mol
则反应的CO2(g)+CH4(g) 2CO(g)+2H2(g)的△H=___________。
2CO(g)+2H2(g)的△H=___________。
(2)工业上,可利用太阳能以CO2为原料制取C,其原理如下图所示:
整个过程中__________(填“Fe3O4”或“FeO”)是反应的催化剂。重整系统中发生的反应为6FeO+CO2 2Fe2O3+C,每生成1molFe3O4,转移电子的物质的量为____________。
2Fe2O3+C,每生成1molFe3O4,转移电子的物质的量为____________。
(3)CO2还可用于合成甲醇,其热化学方程式为:CO2(g)+H2(g) CH3OH(g)+H2O(g)△H<0
CH3OH(g)+H2O(g)△H<0
①该反应的平衡常数表达式为____。
②在恒容的密闭容器中,加入H2和CO2的混合气体,不同温度条件,反应相同时间后,测得甲醇的体积分数甲(CH3OH)如图所示。图中A、B、C、D、E五个点对应的状态中,处于平衡状态的是_______ (填字母),B点和E点的反应速率大小关系为v(B) v(E)(填“>”、“<”、“=”)。
③一定温度下,在甲、乙两个容积相同的密闭容器中,加入H2和CO2的混合气体。
| 容器 |
甲 |
乙 |
| 反应物投入量 |
1molCO2、3molH2 |
amolCO2、bmolH2、cmolCH3OH(g)、cmolH2O(g) |
甲容器平衡后气体的压强为开始时的80%,要使乙容器达平衡时与甲容器达到相同的平衡状态,且起始时反应逆向进行,则c的取值范围为___________。