化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)硅是无机非金属材料的主角。请你举出两种含硅的材料名称 ;铝制品表面有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏。若将氧化铝与氢氧化钠溶液作用,反应的离子方程式为 。
(2)氯气用于漂白时,实际上起漂白作用的物质不是Cl2而是它和水反应生成的
(写化学式)。缺铁性贫血患者补充的Fe2+,通常以硫酸亚铁的形式,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表要包有一层特殊的糖衣,这层糖衣的作用是 。
(3)从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是 (填代号)。
| A.铜和浓硝酸反应 | B.铜和稀硝酸反应 |
| C.氧化铜和硝酸反应 | D.铜先与浓硫酸共热,再加入硝酸钡 |
已知如图所示的可逆反应:A(g)+B(g) C(g)+D(g)ΔH =" Q" kJ/mol
C(g)+D(g)ΔH =" Q" kJ/mol
请回答下列问题:
(1)Q0(填“>”、“<”或“=”);
(2)在某温度下,反应物的起始浓度分别为:c(A)=" 1.0" mol/L,c(B)="2.0" mol/L ;达到平衡后,A的转化率为50%,此时B的转化率为;
(3)若反应温度升高,A的转化率(填“增大”“减小”或“不变”);
(4)若反应温度不变,反应物的起始浓度分别为:c(A)="3.0" mol/L,c(B)=" a" mol/L;达到平衡后,c(D)="1.0" mol/L,则a=;
(5)反应体系中加入催化剂,反应速率增大,则E1的变化是:E1(填“增大”“减小”“不变”),ΔH的变化是:ΔH(填“增大”“减小”“不变”)。
(7分) 科学家一直致力于“人工固氮”的方法研究。
⑴目前合成氨的技术原理为:
该反应的能量变化如图所示。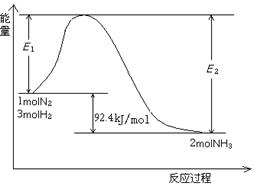
①在反应体系中加入催化剂,反应速率增大,E2的变化是:。(填“增大”、“减小”或“不变”)。
②将一定量的N2(g)和H2(g)放入1L的密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.1 mol,H2为0.3 mol,NH3为0.1 mol。该条件下H2的转化率为。
③欲提高②容器中H2的转化率,下列措施可行的是。
| A.向容器中按原比例再充入原料气 | B.向容器中再充入惰性气体 |
| C.改变反应的催化剂 | D.液化生成物分离出氨 |
⑵1998年希腊亚里士多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传导H+),从而实现了高转化率的电解法合成氨。其实验装置如图所示。阴极的电极反应式为。
⑶根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应: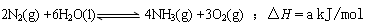
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
| T/K |
303 |
313 |
323 |
| NH3生成量/(10-6mol) |
4.8 |
5.9 |
6.0 |
①合成反应的a_0。(填“大于”、“小于”或“等于”)
②已知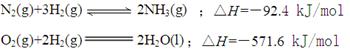
则
如图装置闭合电键时,电流计A的指针将发生偏转。试回答下列问题。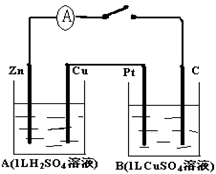
(1)A池是;Zn的电极名称是B池是;Pt的电极名称是
(填电解池、原电池、阴、阳、正、负极等)
(2)写出下列有关反应:
Cu极上电极反应:,C极上电极反应:
(3) B池中的总反应的化学方程式为
(4 )如果要用B池给铁片上镀上一层Cu,则B池应作何改进
(6分)KMnO4溶液与H2C2O4溶液可发生如下反应:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(1)该反应速率开始十分缓慢,一段时间后突然加快,这是因为_____(填化学式)对该反应具有催化作用。
(2)据此原理,可以利用KMnO4溶液来测定H2C2O4溶液的浓度,具体做法如下:
①准确配制0.10mol/L的KMnO4溶液
②将KMnO4溶液盛放在______滴定管中(填“酸式”或“碱式”)
③准确量取25.00mL H2C2O4溶液于锥形瓶中
④进行滴定
滴定终点有什么现象_________________,是否需要指示剂__________(填“是”或“否”)
(3)在下列操作中,会使测定的H2C2O4溶液浓度偏大的是___________。
①盛装KMnO4溶液的滴定管用蒸馏水洗净后未用KMnO4溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③盛装H2C2O4溶液的滴定管用蒸馏水洗净后,未用H2C2O4溶液润洗
④滴定后观察滴定管读数时,视线高于刻度线
(4)滴定时所得的实验数据如下,试计算所测H2C2O4溶液的浓度为_________mol/L
| 实验次数编号 |
待测液体积mL |
滴入的标准液体积(mL) |
| 1 |
25.00 |
28.95 |
| 2 |
25.00 |
25.05 |
| 3 |
25.00 |
24.95 |
(3分)25℃时,有下列四组溶液①0.1mol/L醋酸溶液,②0.1mol/L的盐酸,③pH=13的氢氧化钠溶液,④pH=13的氨水
(1)溶液中的c(H+)大小关系是(填序号,下同)。
(2)其中水的电离程度最大的是。
(3)取等体积的③和④的溶液分别稀释100倍,稀释后溶液的pH关系为③④(填“>”、“=”、“<”)。