下列有关Na2CO3和NaHCO3的叙述中,正确的是
| A.NaHCO3俗名纯碱,Na2CO3俗名苏打 |
| B.受热时,NaHCO3比Na2CO3容易分解 |
| C.NaHCO3溶液显酸性,Na2CO3溶液显碱性 |
| D.NaHCO3和Na2CO3各1mol分别与过量盐酸充分反应,产生CO2的质量不同 |
短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族,Y与W同主族,且X的原子半径小于Y。下列叙述正确的是
| A.原子半径:Y<Z<W | B.Z在化合物中呈+1价 |
| C.Y与W可形成离子化合物 | D.Z的单质不能与X的氧化物反应 |
现用胆矾(CuSO4•5H2O)配制0.1mol·L—1的硫酸铜溶液,下列操作中合理的是
| A.称量时,将胆矾晶体直接放在托盘天平的右盘上 |
| B.准确称取16.0g胆矾,溶于水,所得溶液恢复到室温,再转移至1000mL容量瓶中,定容 |
| C.准确称取25.0g胆矾,溶于水,所得溶液恢复到室温,再转移至1000mL容量瓶中,定容 |
| D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
在pH=1的无色溶液中能大量共存的离子组是
| A.NH4+、Mg2+、SO42-、Cl- | B.Ba2+、K+、OH-、NO3- |
| C.Al3+、Cu2+、SO42-、Cl- | D.Na+、Ca2+、Cl-、CO32- |
下列操作方法或实验装置正确的是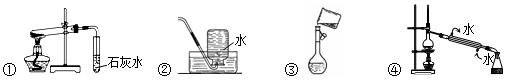
| A.装置①探究NaHCO3的热稳定性 | B.装置②SO2的收集 |
| C.装置③向容量瓶中转移液体 | D.装置④石油蒸馏 |
下列变化中,属于加成反应的是
| A.乙烯使酸性KMnO4溶液褪色 | B.将苯滴入溴水中,振荡后水层接近无色 |
| C.乙烯使溴的四氯化碳溶液褪色 | D.甲烷与氯气混合光照一段时间后黄绿色消失 |