由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。
(1)聚合物F的结构简式是_____________________________________。
(2)D的结构简式是___________________________________________。
(3)由A转化为B的化学反应类型 、由D转化为E的化学反应类型为 。
(4)B转化为C的化学方程式是______________________________________________。
(5)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是_________________________________________。
(6)E有多种同分异构体,其中分子结构中含有碳氧双键,同时1mol该物质与足量的金属钠反应能产生1mol H2,则E的同分异构体可能为_______________________________  。
。
我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾.检验食盐中是否加碘,可利用如下反应:KIO3+KI+H2SO4═K2SO4+I2+H2O.
(1)将上述氧化还原反应的化学方程式配平.
(2)该反应中,氧化剂和还原剂的物质的量之比为.
(3)如果反应中转移0.2mol电子,则生成I2的物质的量为.
(4)利用上述反应检验食盐中是否加碘,所需试剂是(填序号).
①碘水 ②KI溶液 ③淀粉溶液 ④稀硫酸 ⑤AgNO3溶液.
多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成分为BaCO3,且含有铁、镁等离子),制备BaCl2 • 2H2O,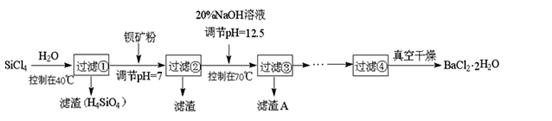
工艺流程如下:
已知:①常温下Fe3+、Mg2+ 完全沉淀的pH分别是3.4、12.4;
②BaCO3的相对分子质量是197; BaCl2 • 2H2O的相对分子质量是244;
(1)SiCl4发生水解反应的化学方程式。
(2)氮化硅(Si3N4)是一种高温结构材料,粉末状的Si3N4可以在高温条件下由SiCl4 蒸
汽与NH3反应得到,请写出该反应的化学方程式。
(3)加钡矿粉调节pH=7的作用是:
①使BaCO3转化为BaCl2
②_______________________________
(4)生成滤渣A的离子方程式________________________________________
(5)BaCl2滤液经____________________、______________________、过滤、洗涤,再经真空干燥后得到BaCl2 • 2H2O
(6)10吨含78.8% BaCO3的钡矿粉理论上最多能生成BaCl2 • 2H2O___________吨。
中学常见反应的化学方程式有A+B→X+Y+H2O或H2O+A+B→X+Y(未配平,反应条件略去),下列问题所涉及反应是上述两个方程式之一。请回答:
(1)常温下,若A为黄绿色气体,B为非金属氧化物,A、B均能使品红溶液褪色,A+B+H2O→X+Y,且相对分子质量X>Y,则该反应的化学方程式________________,检验Y中阴离子的试剂是________________。
(2)若A为常见的金属单质,Y为气态单质,B溶液呈强酸性或强碱性时,A和B反应都能进行。写出A与B反应的离子方程式:;
。
(3)若A为常见的非金属单质,它是构成有机物的基本元素之一,B的溶液为某浓酸,其中A、B的物质的量之比为1∶4,则该反应化学方程式为。
(4)若A、B均为化合物,Y为白色沉淀(不含金属元素),B为引起温室效应的主要气体,写出A与B反应生成Y的离子方程式。
有一瓶澄清溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、Mg2+、I-、NO3-、CO32-、SO42-、AlO2-。取该溶液进行以下实验:
①用PH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;
c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。其中产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如下图所示。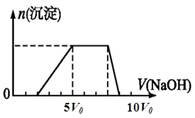
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除的存在。
(2)由②可以证明的存在;同时排除的存在;
(3)由①③可以推知该溶液中一定含有的阳离子是,
它们的物质的量浓度比为。
(4)由④可以证明的存在,同时排除的存在。
在温度T ℃下,某Ba(OH)2稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,向该溶液中逐滴加入NaHSO4溶液,测得混合溶液的部分pH如下表所示:
| 序号 |
氢氧化钡的体积/mL |
硫酸氢钠的体积/mL |
溶液的PH |
| ① |
33.00 |
0.00 |
8 |
| ② |
33.00 |
X |
7 |
| ③ |
33.00 |
33.00 |
6 |
(1)依据题意判断,T ℃________25 ℃(填“大于”、“小于”或“等于”);
(2)b=,X=;
(3)反应③的离子方程式为:;
(4)将此温度下的Ba(OH)2溶液取出1 mL,加水稀释至1L,则稀释后溶液中c(Ba2+):c(OH-)。