下列各组离子能在指定溶液中大量共存的是 ( )
①酸性溶液中:Fe2+,Al3+,NO3-,I-,S2-
②在pH=11的溶液中:Na+,AlO2-,NO3-,S2-,SO32-
③由水电离的c(H+)=1×10-13mol/L的溶液中:Cl-,HCO3-,NO3-,NH4+,S2O32--
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使甲基橙变红的溶液中:Fe3+,MnO4-,NO3-,Na+,SO42-
⑥无色溶液中:K+,Cl-,Na+,H2PO4-,PO43-
| A.①②⑤ | B.①③⑥ | C.②④⑤ | D.①②④ |
下列关于判断过程的方向的说法正确的是( )
| A.所有自发进行的化学反应都是放热反应 |
| B.高温高压下可以使石墨转化为金刚石的过程是自发过程 |
| C.综合考虑焓变和熵变将更适合于所有的过程 |
| D.同一物质的固、液、气三种状态的熵值相同 |
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
| A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C.电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D.镀锌层破损后即对铁制品失去保护作用 |
2010年10月1日,我国在西昌卫星发射中心成功发射“嫦娥二号”。嫦娥二号火箭推进器以联氨(N2H4)为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式为
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O(l);ΔH2=-44 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g);ΔH3=-196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=+817.63 kJ·mol-1 |
| B.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-641.63 kJ·mol-1 |
| C.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=-641.63 kJ·mol-1 |
| D.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-817.63 kJ·mol-1 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O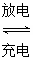 3Zn(OH)2+2Fe(OH)3+4KOH。关于该电池的说法正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。关于该电池的说法正确的是( )
| A.放电时,Zn作负极,发生还原反应 |
| B.放电时,K2FeO4附近溶液pH减小 |
| C.充电时,锌极附近溶液pH减小 |
| D.充电时,阳极电极反应为: |
Fe(OH)3-3e-+5OH-=FeO +4H2O
+4H2O
在208 K、100 kPa时,已知:
2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是( )
| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |