向2 L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3——t4阶段为使用催化剂。观察下图,回答下列问题: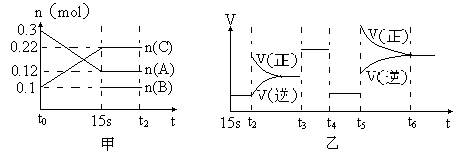
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为 。
(2)乙图中t2时引起平衡移动的条件是 ,t5时引起平衡移动的条件是 。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是 。
(4)该反应的化学方程式可以表示为: ,正反应为 (填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为 。
我国使用最早的合金是_____________,目前用量最大,使用最广泛的合金是___________。合金的硬度一般比它的各成分金属的硬度_________,多数合金的熔点一般比它的各成分金属的熔点___________。镁铝合金投入氢氧化钠溶液中,反应的化学方程式为__________________________,红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为___________________________。
(1)写出电解食盐水的化学方程式:;
写出实验室制取氯气的化学方程式:。
(2)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。这个变色的过程中的Fe2+被(填“氧化”或“还原”)。若榨汁时加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有性。
(3)为防止碘缺乏病,通常在食盐中添加少量碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应。用双线桥标出方程式中电子转移的方向与数目。
5 KI+ KIO3+ 3H2SO4="" 3 I2+ 3 K2SO4+ 3 H2O
此反应中氧化剂和还原剂的物质的量之比是。
有一瓶溶液只含Cl-、CO32—、SO42—、Na+、NH4+、K+、Mg2+七种离子中的某几种。经实验:
 回答下列问题:
回答下列问题: (1) 试分析原溶液中一定含有的离子是 ,一定不含有的离子是
(1) 试分析原溶液中一定含有的离子是 ,一定不含有的离子是  (2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”),
(2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”), 并说明理由。
并说明理由。
(1)现有标准状况下的氮气5.6g,其体积为L,含有氮分子的数目为。
(2)某密闭容器的质量为50 g,当装满CO2气体时,质量为58.8 g,如果装满CH4气
体时,质量为 g。
(3)已知某气体氧化物的分子式为R2O3,在标准状况下,7.6 g该气体的体积是2240 mL ,
则此氧化物的摩尔质量是,R的相对原子质量是。
A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处于同一周期,A、C处于同一主族。C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的4倍。试回答下列问题:
(1)这四种元素分别是:A,B,C,D。
(2)这四种元素中能形成的气态氢化物的稳定性由大到小的顺序是
。(用气态氢化物的化学式表示)
(3)A和B形成的三原子分子的化学式是,B与D形成的既有离子键又含有共价键的化合物的化学式是。
(4)A元素的某氧化物与D元素的某含氧化合物反应生成单质的化学方程式是
。