(4分) 某温度(t℃)时,水的离子积为KW=1×10-13mol2·L-2,则该温度( 选填大于、小于或等于) 25℃,此时水的pH 7(选填大于、小于、等于)其理由是 。
选填大于、小于或等于) 25℃,此时水的pH 7(选填大于、小于、等于)其理由是 。
(1)常温下,0.2 mol·L-1HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,则
①混合溶液中由水电离出的c(H+) (填“>”、“<” 或“=”)原HCl溶液中由水电离出的c(H+)。
②求出混合溶液中下列算式的精确计算结果(填具体数字)。c(Cl-)-c(M+)= mol·L-1;
(2)常温下,若将0.2 mol·L-1MOH溶液与0.1 mol·L-1HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下,MOH的电离程度 (填“大于”、“小于”或“等于”) MCl的水解程度。
(3)常温下,若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH (填“>7”或“< 7”或“无法确定”)。
(4)AgNO3的水溶液呈 (填“酸”、“中”或“碱”)性,原因是(用离子方程式表示) ;实验室在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需的浓度,以 (填“促进”或“抑制”)其水解。
(5)把FeCl3溶液蒸干、灼烧,最后得到的固体产物主要是 。
在一定条件下进行如下反应:aX(g)+bY(g)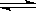 cZ(g)。下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。
cZ(g)。下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。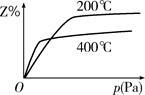
(1)写出该反应的化学平衡常数表达式:K=________。随着温度的升高,K值________(填“增大”“减小”或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明________(填字母)。
| A.X的转化率越高 |
| B.反应进行得越完全 |
| C.达到平衡时X的浓度越大 |
| D.化学反应速率越快 |
(2)如图所示,相同温度下,在甲、乙两容器中各投入1molX、2molY和适量催化剂,甲、乙两容器的初始体积均为1L。甲、乙容器达到平衡所用时间:甲________乙(填“>”“<”或“=”,下同),平衡时X和Y的转化率:甲________乙。
在一个固定体积为2升的密闭容器中,充入2molA和1molB,发生如下反应: 2A(g)+B(g)  3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
①2分钟内用B表示的平均反应速度为 ;
②若容器温度升高,平衡时混合气体的平均摩尔质量减小,则正反应为 (填 “吸热”或“放热”)反应。
肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
(1)写出肼和N2O4反应的热化学方程式______________________。
(2)已知H2O(l)=H2O(g) ΔH3=+44 kJ·mol-1,则表示肼燃烧热的热化学方程式为_______________________________。
五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E周期序数等于E原子最外层电子数。根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是 (用元素符号填写)
(2)乙物质中存在的化学键类型是 。
(3)选用恰当的试剂除去D中少量的E,写出发生反应的化学方程式
(4)化合物乙的电子式
(5)将D、E的单质插入NaOH溶液中,构成原电池,其负极反应是