(1)常温下,0.2 mol·L-1HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,则
①混合溶液中由水电离出的c(H+) (填“>”、“<” 或“=”)原HCl溶液中由水电离出的c(H+)。
②求出混合溶液中下列算式的精确计算结果(填具体数字)。c(Cl-)-c(M+)= mol·L-1;
(2)常温下,若将0.2 mol·L-1MOH溶液与0.1 mol·L-1HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下,MOH的电离程度 (填“大于”、“小于”或“等于”) MCl的水解程度。
(3)常温下,若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH (填“>7”或“< 7”或“无法确定”)。
(4)AgNO3的水溶液呈 (填“酸”、“中”或“碱”)性,原因是(用离子方程式表示) ;实验室在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需的浓度,以 (填“促进”或“抑制”)其水解。
(5)把FeCl3溶液蒸干、灼烧,最后得到的固体产物主要是 。
现有NaCl、Na2SO4、NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀和固体,从而实现阴离子的分离。相应的实验过程可用下图所示:
请回答下列问题:
⑴写出实验流程中下列物质的化学式:试剂X :,沉淀A:,沉淀B:。
⑵上述实验流程中加入过量的Na2CO3的目的是。
⑶按此实验方案得到的溶液3中肯定含有(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的,之后若要获得固体NaNO 3需进行的实验操作是(填操作名称)。
3需进行的实验操作是(填操作名称)。
用双线桥表示下列反应中得失电子的情况,并指明氧化剂、还原剂、氧化产物、还原产物:
3FeO + 10HNO3 ="==" 3Fe(NO3)3+ NO↑ + 5H2O
()()()()
其中,氧化性:__________ > ___________;还原性:___________ > ___________
 胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反
胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反 应的离子方程式:__;如果病人同时患胃溃疡,为防胃壁穿孔,最好用含氢氧化稆的胃药(如胃舒平),反应的离子方程式为:。
应的离子方程式:__;如果病人同时患胃溃疡,为防胃壁穿孔,最好用含氢氧化稆的胃药(如胃舒平),反应的离子方程式为:。
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用下图所法实验装置可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
①a电极材料为___ ____,其电极反应式为_______________________。
____,其电极反应式为_______________________。
②电解液d可以是_______,则白色沉 淀在电极上生成;也可以是_______,
淀在电极上生成;也可以是_______,
则白色沉淀在两极之间的 溶液中生成。
溶液中生成。
A.纯水 B.NaCl 溶液 C.NaOH溶液 D.CuCl2溶液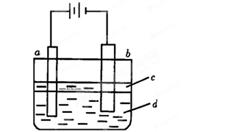
③液体c为苯,其作用是________________,在加入苯之前,对d溶液进行加热处理的目的是____________________。
④为了在短时间内看到白色沉淀,可以采取的措施是____________________。
A.改用稀硫酸做电解液 B.适当增大电源电压
C.适当缩小两电极间距离 D.适当降低电解液温度
⑤若d改为Na2SO4溶液,当电解一段时间,看到 白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为______________________。
白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为______________________。
现有电解质溶液:①Na2CO3②NaHCO3③NaAlO2④CH3COONa ⑤NaOH
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是____________
(填编号,下同)
(2)将上述物质的量浓度均为0.1 mol/L 的五种溶液,稀释相同倍数时,其pH变化最大的是____
(3)在上述五种电解质溶液 中,分别加入AlCl3溶液,无气体产生的是____________
中,分别加入AlCl3溶液,无气体产生的是____________