已知烧杯中装有200g硫酸和硫酸锌混合溶液,其中含硫酸锌12.1g。向烧杯中逐渐加入锌粒,放出气体质量与加入锌粒质量的关系如图14所示。当恰好完全反应时,所得的溶液为不饱和溶液。

请计算:
(1)m的值。
(2)原混合溶液中
的质量分数。
(3)恰好完全反应时,所得溶液中溶质的质量分数
碱石灰是氧化钙和氢氧化钠的固体混合物,是实验室常用的干燥剂。相关信息如下图所示。同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究。
[提出问题]实验室中久置的碱石灰样品的成分是什么?
[进行猜想] 久置的碱石灰样品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分。用化学方程式表示样品中含有Ca(OH)2或Na2CO3可能含有的原因 (写一个)
[探究过程]
试回答下列问题:
(1)操作①的名称是,溶液C中一定含离子。
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有,反应的方程式为。
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是。
[实验结论]
依据上述实验操作过程及现象,综合对滤液和固体成分的探究,下列对样品成分的分析正确的是(填序号)
①样品中一定含NaOH②样品中一定含Na2CO3③样品中含NaOH、CaO中的一种或两种
[拓展延伸]
为测定实验室中一瓶变质的烧碱中NaOH的含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g。请分析计算:
(1)反应产生的CO2的质量为g。
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是多少?(写出计算过程)
(3)用同浓度的硫酸,分别与未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等。从钠元素质量守恒的角度解释其原因是:。
碳酸钠和碳酸氢钠的固体混合物充分加热至恒重,其质量变化如下图所示。另取相同质量的该混合物溶于水得到106.6 g溶液,向该溶液中加入100 g 7.3% 的稀盐酸,恰好完全反应。(已知:2NaHCO3 Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
计算:(1)混合物与盐酸反应生成二氧化碳的质量。(2)所得溶液中溶质的质量分数。
工业利用叠氮酸钠(NaN3)和硝酸钠反应制备纯净的氧化钠,反应的化学方程式是5NaN3+NaNO3=3Na2O+8N2↑。
计算:生产186吨氧化钠理论上需要硝酸钠的质量。
下图是浓盐酸试剂瓶标签的部分内容。请回答: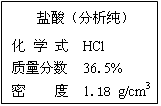
① 欲配制200g溶质质量分数为3.65%的稀盐酸,需要这种浓盐酸g,体积为mL。
②用①中所得稀盐酸与足量锌粒反应,请根据化学方程式计算最多可得氢气的质量
为测定石灰石中碳酸钙的质量分数,化学兴趣小组的同学设计了以下方案:将94.4g稀盐酸加入到15g石灰石样品中,恰好完全反应。生成的二氧化碳气体全部用足量的NaOH溶液吸收,NaOH溶液增加的质量随时间变化如下表:(友情提示:石灰石中的杂质不参加反应且难溶于水)
| 时间(min) |
t1 |
t2 |
t3 |
t4 |
t5 |
t6 |
t7 |
t8 |
| 氢氧化钠溶液增加的质量(g) |
1.5 |
2 |
2.5 |
3 |
3.5 |
4 |
4.4 |
4.4 |
求:(1)最终生成CO2的质量;
(2)样品中CaCO3的质量分数(计算结果精确到0.1%);
(3)将石灰石与稀盐酸反应后的剩余物质进行过滤,再向滤液中加入多少克水可以得到溶质质量分数为10%的CaCl2溶液。