下列反应的离子方程式不正确的是
| A.向NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| C.足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O=2NaHCO3↓ |
| D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
对于可逆反应2AB3(g) 2A(g) + 3B2(g) ΔH>0下列图象不正确的是
2A(g) + 3B2(g) ΔH>0下列图象不正确的是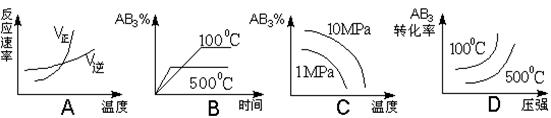
在一密闭容器中有如下反应:L (s) + a G (g) b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断
b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断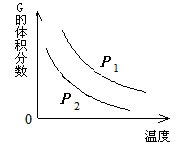
| A.正反应为放热反应 |
| B.化学方程式中的计量数a > b |
| C.G的转化率随温度升高而减小 |
| D.增大压强,容器内气体质量不变 |
在一密闭容器中,反应aA(g)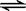 bB(g),达到平衡后,保持温度不变,将容器体积增加1倍,当达到新的平衡时,B的浓度是原来的70%,则
bB(g),达到平衡后,保持温度不变,将容器体积增加1倍,当达到新的平衡时,B的浓度是原来的70%,则
| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 | D.化学计量数关系:a>b |
图1为某化学反应的速率与时间的关系示意图。下列有关t1时刻改变条件的说法正确的是()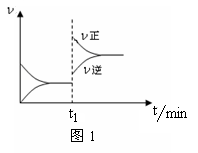
A.2SO2(g)+O2(g)  2SO3(g) ΔH<0,t1时刻升高温度 2SO3(g) ΔH<0,t1时刻升高温度 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2浓度 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2浓度 |
C.H2O(g)+CO(g)  H2(g)+CO2(g) ΔH>0, t1时刻增大压强 H2(g)+CO2(g) ΔH>0, t1时刻增大压强 |
D.C(s)+H2O(g) CO(g)+H2(g) ΔH>0,t1时刻升高温度 CO(g)+H2(g) ΔH>0,t1时刻升高温度 |
COCl2(g) 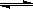 CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压时通入惰性气体,能提高COCl2转化率的是()
CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压时通入惰性气体,能提高COCl2转化率的是()
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |