有两个无标签的试剂瓶,分别盛有Na2CO3、NaHCO3固体,有四位同学为鉴别它们采用了以下不同方法,其中可行的是
| A.分别将它们配制成溶液,再加入澄清石灰水 |
| B.分别将它们配制成溶液,再加入NaOH溶液 |
| C.分别将它们配制成溶液,再进行焰色反应 |
| D.分别加热,再用澄清石灰水检验是否有气体产生 |
水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32—+O2+xOH—=Fe3O4+S4O62— +2H2O,下列说法正确的是
| A.x=2 |
| B.参加反应的Fe2+全部做还原剂 |
| C.每生成1mol Fe3O4,反应转移的电子总数为4mol |
| D.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol |
下列变化属于吸热反应的是:
①液态水汽化②将胆矾加热变为白色粉末③浓硫酸稀释④氯酸钾分解制氧气
⑤生石灰与水反应生成熟石灰⑤I2→I+I⑥H+Cl→HCl⑦氢气还原氧化铜
| A.①②④⑤ | B.②④⑤⑦ | C.①④⑤③ | D.②④⑦ |
在一个不传热的固定容积的密闭容器中,可逆反应: N2+3H2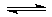 2NH3 ,达到平衡的标志是
2NH3 ,达到平衡的标志是
①反应速率v(N2):v(H2):v(NH3) =" 1" : 3 : 2②各组分的物质的 量浓度不再改变
量浓度不再改变
③体系的压强不再发生变化④混合气体的密度不变
⑤体系的温度不再发生变化⑥ 2V(N2)正= V(NH3)
⑦单位时间内3 mol H—H断键反应同时2 mol N—H也断键反应
| A.①、②、③、⑤、⑥ | B.②、③、⑤、⑥ |
| C.②、③、⑤、⑥、⑦ | D.②、③、④、⑥、⑦ |
C6H14中含有3个“—CH3”的结构种数
| A.1 | B.2 | C.3 | D.4 |
甲烷在高温条件下可发生分解:2CH4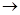 C2H2+3H2,现使甲烷分解得到的混合物的气体对氦的相对密度为2.5,则甲烷的分解率是:
C2H2+3H2,现使甲烷分解得到的混合物的气体对氦的相对密度为2.5,则甲烷的分解率是:
| A.50% | B.60% | C.70% | D.80% |