将100 mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。下列判断错误的是( )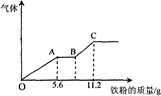
| A.OA段产生的气体是NO,BC段产生的气体是H2 |
| B.A点对应消耗NO3-物质的量为0.1 mol |
| C.B点对应的消耗铁粉的质量为8.4 g |
| D.原混合酸溶液中H2SO4浓度为2.0 mol·L-1 |
某铁的“氧化物”样品,用5 mol/L盐酸50 mL恰好完全溶解,所得溶液还能吸收标准状况下0.56 L氯气,使其中Fe2+全部转化为Fe3+。该样品可能的化学式是
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |
要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4 ③加入少量KSCN溶液
| A.①③ | B.③② | C.③① | D.①②③ |
下列说法正确的是
| A.pH=6的降雨是酸雨 |
| B.氯气泄漏后应顺风向低处跑 |
| C.SO2和HClO都具有漂白性,两者的漂白原理相同 |
| D.我国城市环境中的大气污染物主要有SO2、NO2、CO、可吸入颗粒物等 |
40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如下图所示。下列说法不正确的是
| A.在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-) |
| B.不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) |
C.随着CO2的通入, 不断增大 不断增大 |
| D.在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成 |
室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是
| 加入的物质 |
结论 |
|
| A |
50mL 1 mol/LH2SO4 |
反应结束后,c(Na+)=c(SO42-) |
| B |
0.05molCaO |
溶液中c(OH-) /c(HCO3-) 增大 |
| C |
50mL H2O |
由水电离出的c(H+)·c(OH—)不变 |
| D |
0.1molNaHSO4固体 |
反应完全后,溶液pH减小,c(Na+)不变 |