实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律的摆放在实验桌上,如下图。做“硫酸的性质”的实验时,某同学取用BaCl2溶液后,应把它放回的位置是
已知丁基有4种,据此不必试写,即可断定C5H10O的醛应有()
| A.3种 | B.4种 | C.5种 | D.6种 |
下列醇中能发生消去反应,但不能被催化氧化成相同碳原子数的醛或酮的是()
| A.甲醇 | B.2-甲基-2-丁醇 |
| C.2-丙醇 | D.3,3-二甲基-2-丁醇 |
下列四个反应中,与其他三个反应类型不同的是()
A.CH3CHO+2Cu(OH)2 CH3COOH+Cu2O↓+2H2O CH3COOH+Cu2O↓+2H2O |
B.CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O CH3COONH4+2Ag↓+3NH3+H2O |
C.CH3CHO+H2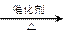 CH3CH2OH CH3CH2OH |
D.CH3CHO+CuO CH3COOH+Cu CH3COOH+Cu |
己烯雌酚是一种激素类药物,结构如下,下列有关叙述中不正确的是()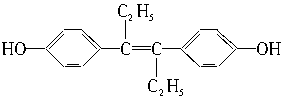
| A.它易溶于有机溶剂 |
| B.可与NaOH和Na2CO3发生反应 |
| C.1mol该有机物可以与5molBr2发生反应 |
| D.该有机物分子中,一定有14个碳原子共平面 |
.下列有关苯酚的叙述中,正确的是()
①纯净的苯酚是粉红色晶体,65℃以上时与水混溶 ②苯酚沾在皮肤上应用酒精洗涤 ③苯酚有毒,不能配成洗涤剂和软膏 ④苯酚比苯容易发生苯环上的取代反应
| A.①③ | B.②④ | C.①④ | D.②③ |