在恒温、恒容的条件下,有反应2A(g)+2B(g)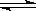 C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2 mol/L和6mol/L。则以下叙述正确的是
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2 mol/L和6mol/L。则以下叙述正确的是
A.两途径最终达到平衡时,体系内混合气的压强相同
B.两途径最终达到平衡时,体系内混合气的百分组成不同
C.达平衡时,途径Ⅰ的反应速率v(A)等于途径Ⅱ的反应速率v(A)
D.达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的1/2
100 mL 6 mol·L-1H2SO4跟0.8 mol锌片反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量
| A.硝酸钠固体 | B.硝酸钠溶液 | C.6 mol·L-1硫酸氢钾溶液 | D.醋酸钠固体 |
下列说法中正确的是
| A.凡是放热反应都是自发的,由于吸热反应都是非自发的 |
| B.自发反应在恰当条件下才能实现 |
| C.自发反应在任何条件下都能实现 |
| D.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
下列物质按纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是
| A.纯盐酸、水煤气、硫酸、醋酸、干冰 |
| B.冰醋酸、玻璃、硫酸钡、氢氟酸、乙醇 |
| C.单甘油酯、冰水混合物、苛性钠、氢硫酸、三氧化硫 |
| D.绿矾、漂白粉、次氯酸、氯化钾、氯气 |
反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后 ,水蒸气的物质的量增加了0.45mol,则此反应的平均速率可表示为
,水蒸气的物质的量增加了0.45mol,则此反应的平均速率可表示为
| A.v (NH3)=0.01mol/(Ls) | B.v (O2)=0.001mol/(Ls) |
| C.v (NO)=0.001mol/(Ls) | D.v (H2O)=0.0 45mol/(Ls) 45mol/(Ls) |
直接提供电能的反应一般是放热反应,下列反应中能提供电能的是
| A.Ba(OH)2·8H2O与NH4Cl反应 | B.氢氧化钠与稀盐酸反应 |
| C.灼热的炭与CO2反应 | D.H2与Cl2燃烧反应 |