(10分)25时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因 (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+) 0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填“>”、“<”或“=”)
(3)求出混合液中下列算式的精确计算结果(填具体数字):
c (Na+)-c (A-)= mol·L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH 7 (填“>”、“<”或“=”);
(5)将相同温度下相同浓度的四种溶液:
| A.NH3·H2O | B.NH4A | C.NH4HSO4 | D.NH4Cl按NH4+浓度由大到小的顺序排列(填序号) |
右下图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)在卡片上,叙述合理的是__________________(填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是____________________________________________________。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因________________。
(4)如果把硫酸换成硫酸铜溶液,猜测_________(填“锌极”或“铜极”)变粗,原因是__________________(用电极方程式表示)。
下表为元素周期表的一部分,请参照元素①-⑧
在表中的位置,用化学用语回答下列问题:
| 族 周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA[ |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
(1)⑧的原子结构示意图为_________。
(2)②的气态氢化物分子的结构式为_____________。
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是。(填化学式)
(4)⑤、⑥元素的金属性强弱依次为___________。(填“增大”、“减小”或“不变”)
(5)④、⑤、⑥的形成的简单离子半径依次___________。(填“增大”、“减小”或“不变”)
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:,形成的晶体是晶体。
已知一定条件下,CO(g) + H2O (g)  CO2 (g)+ H2 (g)反应过程能量变化如右图所示,该反应为反应(填“吸热”或“放热”),反应的热化学方程式为:。
CO2 (g)+ H2 (g)反应过程能量变化如右图所示,该反应为反应(填“吸热”或“放热”),反应的热化学方程式为:。
将下列物质进行分类:①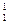 H与
H与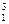 H②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
H②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
(1)互为同位素的是(填编号、下同);
(2)互为同素异形体的是;
(3)互为同分异构体的是;
A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,D是具有果香气味的烃的衍生物。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
⑴A→B的反应类型是_______________;B、D中官能团的名称分别是_______、________;
⑵写出反应B+C→D的化学方程式:_______________________________________。
⑶丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式:____________________________________________。
⑷人在做过剧烈运动后,有一段时间腿和胳膊感到有酸胀或疼痛的感觉。原因之一是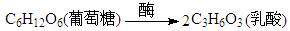 。
。
已知乳酸分子中含有与B、C中相同的官能团,且有一个甲基,则乳酸的结构简式是,90 g乳酸与足量金属钠完全反应产生的气体在标准状况下的体积是L