500℃时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中H2、N2和NH3物质的量变化如右图所示,分析图像完成下列填空:
(1)0—10分钟,N2的平均反应速率为 ___________mol·L-1·min-1, 0—10分钟与10到20分钟两个时间段中,N2的反应速率之比为_________。反应在第10min可能改变的条件是____________,运用图像信息说明该条件不是升温的原因是____________。
(2)计算500℃时,反应N2+3H2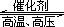 2NH3的平衡常数K的数值为_____________。保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将_______(填“增大”或“减小”或“不变”)。保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态_____(填“大”或“小”或“不变”)。
2NH3的平衡常数K的数值为_____________。保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将_______(填“增大”或“减小”或“不变”)。保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态_____(填“大”或“小”或“不变”)。
(3)在图中画出25min—40min时间段内N2的物质的量的变化图像。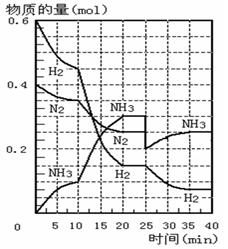
下列选项合理的是()
A.pH皆等于3 的两种溶液都稀释100倍后,pH都为5
B.10mL 0.02mol/L HCl溶液与10mL 0.02mol/L Ba(OH) 2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7
C.在0.1mol/L某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
D.室温下,在一定量稀氨水中逐滴滴入稀盐酸,对于所得溶液中离子浓度大小关系
可能是:c(NH4+)>c(Cl—)>c(OH—)>c(H+)
NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.用石墨电极电解Ca(NO3)2溶液,当转移电子数为0.2 NA时,阴极析出4 g金属 |
| B.0.1 mol24Mg32S晶体中所含中子总数为2.8 NA |
| C.常温下含有NA个NO2、N2O4分子的混合气体,温度降至标准状况,其体积约为22.4 L |
| D.在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2 NA |
下列有关有机物的说法正确的是()
| A.甲烷、乙烯和苯在工业上都可通过石油分馏得到。 |
| B.米酒变酸的过程涉及了氧化反应。 |
| C.乙烯和聚丙烯都能与氢气在一定条件下发生加成反应。 |
| D.淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应。 |
化学与生产、生活、社会密切相关。下列说法中不正确的是()
| A.“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致。 |
| B.绿色化学的核心是从源头上消除工业生产对环境的污染。 |
| C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈。 |
| D.华商科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅。 |
铁锈的主要成分为Fe2O3· xH2O,已知298K时,由单质生成Fe2O3的ΔH=-824 kJ/mol且ΔH-T?S=-742.4 kJ/mol。计算说明在-150℃的空气中铁是否发生锈蚀?