制印刷电路时常用氯化铁溶液作为“腐蚀液”。铜被氯化铁溶液腐蚀的方程式为:2FeCl3+Cu=2FeCl2+CuCl2;FeCl3溶液也能与铁反应:2FeCl3+Fe = 3FeCl2;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部不可能出现的是
| A.有铜无铁 | B.有铁无铜 |
| C.有铁有铜 | D.无铁无铜 |
已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:
若在反应中消耗了1 mol乙烷(反应物),则有关该反应的说法正确的是
| A.该反应放出251.2 kJ的热量 | B.该反应吸收251.2 kJ的热量 |
| C.该反应放出125.6 kJ的热量 | D.该反应吸收125.6 kJ的热量 |
下列热化学方程式中,正确的是
| A.甲烷的燃烧热为 890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1 |
B.500℃、30MPa 下,将0.5mol N2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) △H = -38.6 kJ·mol-1 2NH3(g) △H = -38.6 kJ·mol-1 |
| C.HCl 和NaOH 反应的中和热△H =" -57.3" kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热△H = 2×(-57.3)kJ·mol -1 |
| D.在101 kPa 时,2gH2完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H = -571.6 kJ·mol-1 |
周期表中关于主族元素性质的下列叙述不正确的是
| A.主族序数等于原子最外层电子数 |
| B.主族元素最高正化合价等于最外层电子数 |
| C.第n主族元素其最高正化合价为+n价,最低负化合价绝对值为8-n(n≥4) |
| D.第n主族元素其最高价氧化物分子式为R2On,氢化物分子式为RHn(n≥4) |
与图像有关的叙述,正确的是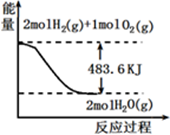
| A.表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量 |
| B.表示的热化学方程式为:H2(g)+ 1/2 O2(g) =H2O(g) △H=-241.8 kJ·mol-1 |
| C.H2O(g)的能量低于H2(g)和O2(g)的能量之和 |
| D.表示2 mol H2(g)所具有的能量一定比2 mol气态水所具有的能量多483.6 kJ |
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子电子层结构。则下列有关说法中错误的是
| A.1 mol NH5中含有5NA个N-H键(NA表示阿伏加德罗常数的值) |
| B.NH5中既有共价键又有离子键 |
C.NH5的电子式为 |
| D.它与水反应的化学方程式为NH5+H2O=NH3·H2O+H2↑ |