合成氨反应为:N2(g)+3H2(g) 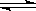 2NH3(g)。图1表示在一定的温度下此反应过程中
2NH3(g)。图1表示在一定的温度下此反应过程中
的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。
图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
下列说法正确的是:
| A.该反应为自发反应,由图1可得加入适当的催化剂,E和△H都减小 |
| B.图2中0~10min内该反应的平均速率v(H2)=0.045mol·L-1·min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d |
| C.图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 |
| D.图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |
下列关于化合物的叙述,正确的是
A.纤维素是植物细胞壁的主要成分,它的基本组成单位是葡萄糖
B.动物细胞间质的物质中主要成分是蛋白质,可用胃蛋白酶处理动物组织
C.DNA是生物的主要遗传物质,它的组成元素有C、H、O、N,部分含S、P
D.磷脂是细胞膜的主要成分,也是线粒体、中心体、叶绿体等生物膜的主要成分
向一个体积可变的密闭容器中充入4mol A、1mol B,发生如下反应:4A(g)+B(s)3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0.3mol·L-1。请填写下列空白:
(1)若容器体积为10L,反应经2min达平衡,则以A物质浓度变化表示的化学反应速率为 ,达平衡时A物质的转化率为 。
(2)若压缩容器增大压强,则逆反应的速率 ,容器中D的体积分数 (填“增大”“减小”或“不变”)。
(3)若相对分子质量M(B)>3M(C),温度升高时混合气体的平均相对分子质量减小,则正反应 (填“吸热”或“放热”)。
(4)在最初的容器中改充1.5mol C、4.4mol D,温度保持不变,要使反应达平衡时D的浓度为0.6mol·L-1,则容器的体积是 L。
下图中横坐标表示完全燃烧时耗用可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示消耗O2的物质的量n(O2),A、B是两种可燃性气体,C是A和B的混合气体,则C中n(A)∶n(B)为
A.2∶1 B.1∶2 C.1∶1 D.任意比
将14g铜银合金与足量的一定浓度的硝酸溶液反应,把放出的气体与标准状况下体积为1.12L的O2混合后再通入水中,恰好全部被吸收,则合金中铜的质量为
| A.3.2g | B.4.8g | C.6.4g | D.10.8g |
下列有关热化学方程式及其叙述正确的是
| A.氢气的燃烧热为285.5kJ/mo1,则水电解的热化学方程式为: 2H2O(l)===2H2(g)+O2(g);ΔH=+285.5kJ/mol |
| B.1mol甲烷完全燃烧生成CO2和H2O(l)时放出890kJ热量,它的热化学方程式为1/2CH4(g)+O2(g)===1/2CO2(g)+H2O(l);ΔH=-445kJ/mol |
| C.已知2C(s)+O2(g)===2CO(g);ΔH=-221kJ·mol-1,则C的燃烧热为110.5kJ/mol |
| D.HF与NaOH溶液反应:H+(aq)+OH—(aq)===H2O(l);ΔH= -57.3kJ/mol |