实验室配制氯化亚铁溶液时,为了防止其氧化,常加入的物质是
| A.Fe | B.Zn | C.Al | D.HCl |
被称之为“软电池”的纸质电池,其电池总反应为Zn+2MnO2+H2O ZnO+2MnO(OH)。下列说法正确的是( )
ZnO+2MnO(OH)。下列说法正确的是( )
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化剂作用 |
| C.当65 g Zn完全溶解时,流经电极的电子为1mol |
D.电池正极反应式为2MnO2+2e-+2H2O 2MnO(OH)+2OH- 2MnO(OH)+2OH- |
将如图所示实验装置的K闭合,下列判断正确的是( )
A.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| B.片刻后可观察到滤纸b点变红色 |
| C.片刻后甲池中c(SO42-)增大 |
D. 电极上发生还原反应 电极上发生还原反应 |
不能用Fe+H2SO4=FeSO4+H2↑表示的是( )
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
| C.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| D.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
如图所示,U形管中装入含有紫色石蕊的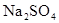 溶液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:()
溶液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:()
| A.蓝、紫、红 |
| B.红、蓝、紫 |
| C.红、紫、蓝 |
| D.蓝、红、紫 |
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、 B、D、E金属性由强到弱的顺序为()
A、D﹥A﹥B﹥E B、D﹥E﹥A﹥B
C、A﹥B﹥D﹥E D、A﹥B﹥E﹥D