已知B是常见金属单质,E为常见非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答:
(1)写出化学式:A____________;E______________;L______________。
(2)反应①的离子方程式:___________________________________。
(3)反应②,工业上采取的反应条件是________________________。
(4)反应③,工业上采取的操作不是K直接与H反应,原因是__________________。
(5)每生成1 mol K, 反应放出98.3 kJ热量,该反应的热化学方程式为:
反应放出98.3 kJ热量,该反应的热化学方程式为:
___________________________________________ ________________________。
________________________。
)已知砒霜As2O3与Zn可以发生如下反应:
As2O3+6Zn+6H2SO4====2AsH3+6ZnSO4+3H2O
(1)请用双线桥法标出电子转移的方向和数目:
。
(2)As2O3在上述反应中显示的性质是 。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(3)该反应的氧化产物是 ,还原产物是 。
(4)若生成0.1 mol AsH3,则转移的电子数为 。
已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO ②N2O3 ③N2O4 ④HNO3 ⑤NH3 ⑥N2O中:
(1)氮元素只能作还原剂的是 (填序号,下同)。
(2)可能是HNO2还原产物的是 。
(3)不可能是N2的氧化产物的是 。
(4)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
。
有反应:
①2H2O+Cl2+SO2====H2SO4+2HCl
②2KMnO4+16HCl====2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)两反应中的氧化剂的氧化性强弱顺序为 ,
还原剂的还原性强弱顺序为 。
(2)反应①中氧化产物和还原产物质量比为 。
一学生设计了如下实验方法分离NaCl、CaCl2两种固体混合物: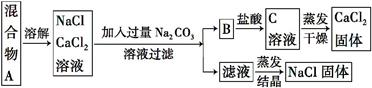
填空回答下列问题
(1)B是 (写化学式)。
(2)按此实验方案得到NaCl,经分析含有杂质,是因为上述方案中某一步设计有错误,这一步正确设计方案应是 。
(3)若要测定该样品中NaCl、CaCl2的质量比,可称量干燥的B和另一种物质的质量,这种物质是 。
(1)阅读、分析下列两个材料:
材料一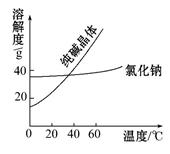
材料二
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
溶解性 |
| 乙二醇 |
-11.5 |
198 |
1.11 |
易溶于水和乙醇 |
| 丙三醇 |
17.9 |
290 |
1.26 |
能跟水、酒精以任意比互溶 |
回答下列问题(填序号):
A.蒸馏法 B.萃取法
C.“溶解、结晶、过滤”的方法 D.分液法
①将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用 ;
②将乙二醇和丙三醇相互分离的最佳方法是 。
(2)阅读材料三。
材料三 在溶解性方面,Br2(溴)与I2很相似,其稀的水溶液显黄色。在实验室里从溴水(Br2的水溶液)中提取Br2和提取I2的方法相似。
回答下列问题:
①常用的提取方法是 ,化学试剂是 ,最主要的仪器是 。
②若观察发现提取Br2以后的水还有颜色,解决该问题的方法是 。