碳和碳的化合物在生产生活实际中应用广泛。运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka = 4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;
4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;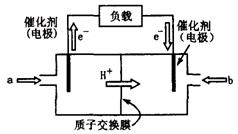
(2)上图为常用笔记本电脑所用的甲醇质子交换膜燃料电池的结构示 意图。电池总反应为2CH3OH+3O2
意图。电池总反应为2CH3OH+3O2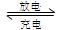 2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;
2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;
(3)CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置。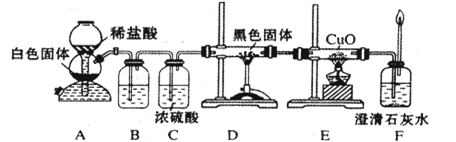
已知:C + H2O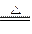 CO+H2 CO + H2O
CO+H2 CO + H2O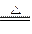 CO2 +
CO2 +  H2 C + CO2
H2 C + CO2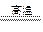 2CO
2CO
试回答下列问题:
①装置B中最适宜的试剂是 ,必须用装置C吸收气体中的水蒸气的理由是 ;
②根据该实验中的 现象,可证明CO具有还原性;
③若要根据装置F中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置 与 之间(填字母标号)连接下图中的 装置(选填序号)。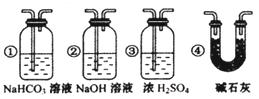
电子工业使用的印刷线路板,是在敷有铜膜的塑料板上以涂料保护所需的线路,然后用FeCl3的溶液与未受保护的铜膜反应以去掉铜,腐蚀后的废液中含有大量的Cu2+。为了回收这一部分Cu2+并制成硫酸铜晶体(CuSO4·5H2O),常用如下步骤:
①向废液中加过量的铁屑,搅拌,静置;②滤出固体物质;③将滤出的固体物质加热煅烧;④把煅烧后的物质放在硫酸中溶解;⑤调节溶液的pH在3.4—4之间,使Fe(OH)3沉淀完全,过滤;⑥浓缩滤液,析出晶体;⑦将过滤得到的晶体溶解,再结晶。
(1)上述③步操作所得煅烧产物成分是_______________。
A.CuO B.CuO和FeO C.CuO和Fe2O3D.CuO和Fe3O4
(2)上述第⑤步操作中,调节溶液的pH宜加入的物质是_______________。
A.氧化铜粉末 B.NaOH溶液 C.稀氨水 D.Na2CO3
(3)上述第⑥步操作中,用浓缩滤液而不用蒸干溶液的主要原因是_______________。
A.蒸干所得到的物质可能含有无水硫酸铜
B.温度升高CuSO4溶解度增大
C.温度升高Cu2+被还原为Cu
D.温度升高CuSO4分解
现给你一试管二氧化氮,其他药品和仪器自选。试设计实验,要求尽可能多地使二氧化氮被水吸收。
| 实验步骤 |
现象 |
解释(可用化学方程式表示) |
|
| (1) |
|||
| (2) |
|||
| (3) |
某学生做钠在氯气中燃烧的实验时,使用了崭新的铜制燃烧匙,当钠燃烧时,除了观察到有白烟外,还有少量棕色的烟,能说明这个现象的化学方程式为
__________________,___________________________;将上述反应得到的固体溶于水后再加入NaOH溶液,产生少量蓝色沉淀,该反应的离子方程式为:
__________________________。
吸烟对健康有害,科学实验表明:香烟所产生的烟雾中至少有300多种化合物对人体有不同的危害。为了鉴定该烟雾中是否存在CO2和CO,将香烟燃烧产物的烟雾进行适当处理后,依次通过足量以下试剂:①澄清石灰水;②浓硫酸;③灼热的黑色氧化铜粉末;④澄清石灰水。发现①④中澄清石灰水变浑浊,其他无明显现象。试完成下列问题:
(1)①中现象说明______________________________________________________________。
(2)烟雾中(填“存在”或“不存在”)CO,作出此判断所依据的实验现象为____________。
(3)③中无明显变化的原因可能是
_________________________________________________。
实验室里若用如图1所示装置制取氨气,试用表格形式列出图中装置的错误之处,并用文字简要说明如何改正。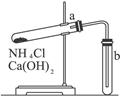
图1