烃的含氧衍生物A,能发生如下图所示的变化。在同温同压下,A蒸气的密度是H2密度的66倍,其中氧元素的质量分数为12.1%;B的化学式为C9H8O2;C能使溴的四氯化碳溶液褪色,与Na反应放出H2;D不含甲基,在一定条件下能发生消去反应。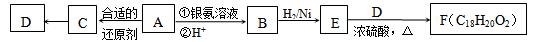
请填写下列空白:
(1)A分子中的含氧官能团的名称为 ,C的结构简式是 。
(2)C→D的反应类型是 (填标号)。
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
(3)D+E→F的化学方程式是 。
(4)与D分子式相同,其中能与金属钠反应且苯环上有一个取代基(包括D)的同分异构体
有 种,写出其中一种含有2个甲基的结构简式
(5)A~F六种化合物中:
①除C外,能与金属钠反应,但不能与氢氧化钠溶液反应的是 (填标号,下同);
②燃烧时消耗的氧气和生成的CO2、H2O之间物质的量之比为11:9:5的是 。
催化剂的研究使许多物质出现了新的化学反应。例如烯烃A在苯中用一种特殊催化剂处理时,生成两种新的烯烃:烯烃B、烯烃C,用反应式可表示为如下:2A B+C
B+C
(1)若A为R1CH=CHR2,B为R1CH=CHR1,试写出上述反应的化学方程式:
(2)对上述反应提出两种可能的反应机理(虚线表示断键位置):
机理a:R1CH=CH——R2
R1——CH=CHR2 B+C
B+C
你认为机理b是(用虚线标明具体的断键位置)
R1——CH=CH——R2+ R1——CH=CH——R2 B+C
B+C
(3)结合你所学,证明是机理a还是机理b,你采用的方法是:
环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂)

回答下列问题:
(1)环烷烃与是同分异构体。
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是(填名称),判断依据为。
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为(不需注明反应条件)。
(4)写出鉴别环丙烷与丙烯的一种方法,试剂;现象与结论。
按要求填空:
(1)(CH3CH2)2C(CH3)2的系统命名为;
(2)2-甲基-1,3-丁二烯的键线式;
(3)有机物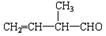 发生加聚反应后,所得产物的结构简式为:
发生加聚反应后,所得产物的结构简式为:
(4)1,3-丁二烯与适量溴单质(60℃)的反应:;
(5) 甲苯→TNT:;
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5 L,回答下列问题
(1 )简述该实验的主要实验步骤
)简述该实验的主要实验步骤
(2)所需仪器为:容量瓶 (规格:)、托盘天平、还需要那些实验仪器才能完成该实验,请写出:。
(3)试分析下列操作对所配溶液的浓度有何影响及造成该影响的原因。
①配制前容量瓶洗涤后没烘干,对所配溶液浓度的影响是(偏大、偏小、无影响。以下同)
②未洗涤烧杯和玻璃棒,对所配溶液浓度的影响:。
③为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至溶量瓶定容。对所配溶液浓度的影响:。
④定容后,加盖倒转摇匀后,发现溶面 低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响。
低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响。
粗食盐中除含有钙离子(CaCl2)、镁离子(MgCl2)、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯 ;②固定铁圈位置 ;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热。其正确的操作顺序为。
何时停止加热。
(2)如何运用最简方法检验溶液中有无SO42-离子,所用试剂。如何检验SO42-离子是否除净简单操作为。
(3)粗食盐中除去钙离子所用试剂为。化学反应方程式
(4)粗食盐中除去镁离子所用试剂为。化学反应方程式