设NA为阿伏加德罗常数的数值,下列说法错误的是
| A.0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.2 NA |
| B.在含有4mol C—C键的金刚石晶体中,碳原子数目为2NA |
| C.20g D2O中含有的质子数目为10NA |
| D.标准状况下,5.6L水中含有的分子数为0.25NA |
下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 |
实验操作 |
实验目的或结论 |
| A |
将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 |
检验水解产物中的溴离子 |
| B |
向苯乙烯中加入酸性高锰酸钾,高锰酸钾褪色 |
说明苯乙烯是苯的同系物 |
| C |
C2H5OH与浓硫酸170℃共热,制得的气体通人酸性KMnO4溶液 |
检验制得气体是否为乙烯 |
| D |
向苯和酒精的混合液中加入金属钠 |
确定苯中是否有酒精 |
绿原酸是咖啡的热水提取液成分之一,结构简式如图,关于绿原酸判断正确的是( )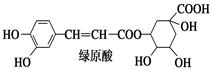
| A.分子中所有的碳原子均可能在同一平面内 |
| B.1 mol绿原酸与足量溴水反应,最多消耗2.5 mol Br2 |
| C.1 mol绿原酸与足量NaOH溶液反应,最多消耗4 mol NaOH |
| D.绿原酸水解产物均可以与FeCl3溶液发生显色反应 |
某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,则这种烃可能是( )
①分子中含有7个碳原子的芳香烃 ②分子中含有4个碳原子的烷烃 ③分子中含有12个氢原子的烷烃 ④分子中含有8个碳原子的烷烃( )
| A.①② | B.②③ | C.③④ | D.②④ |
下列除杂质(括号内为杂质)的实验设计不能达到预期目的是()
| A.乙烷(乙烯):溴水,洗气 | B.甲苯(苯酚):浓溴水,过滤 |
| C.溴乙烷(乙醇):Na2CO3溶液,分液 | D.乙醇(乙酸):碱石灰,蒸馏 |
下列说法正确的是( )
| A.分子式为CH4O和C2H6O的物质一定互为同系物 |
| B.甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
| C.苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸钠 |
D.1 mol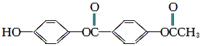 与过量的NaOH溶液加热充分反应,能消耗 与过量的NaOH溶液加热充分反应,能消耗 |
5 mol NaOH