某科研机构用含氯的有机物A合成棉织物免烫抗皱整理剂M,设计合成路线如下(部分反应试剂和条件未注明):
已知:
①用质谱法测得D的相对分子质量在90~110之间,且氧元素的质量分数为0.615;E比D的相对分子质量大28,核磁共振氢谱显示E分子内有2种不同环境的氢原子,其个数比为3 :1。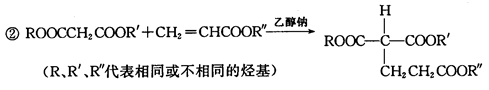
回答下列问题:
(1)A分子中的含氧官能团的名称是____________,G→H的反应类型是____________。
(2)D的分子式为________________;E的结构简式为________________。
(3)H→J反应的化学方程式是______________________。
(4)J在一定条件下可以合成高分子化合物,该高分子化合物结构简式是____________。
(5)已知1 mol E与2mol J反应生成l mol M,则M的结构简式是_______________。
(6)写出与A具有相同官能团的A的所有同分异构体的结构简式___________________________________________________.
下表是元素周期表的一部分。
| 周期族 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 一 |
A |
|||||||
| 二 |
D |
F |
H |
|||||
| 三 |
B |
C |
E |
G |
根据A—H元素在周期表中的位置,用化学式填写下列空白。
(1)单质中氧化性最强的是________________,还原性最强的是________________,化学性质最不活泼的是________________。
(2)最高价氧化物对应水化物的酸性最强的酸是________________________,最稳定的氢化物是________________。
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列为________________。
(4)D、E、F三种元素按原子半径由大到小的顺序排列为________________。
(5)A的氧化物常温下呈____________态,它和B的单质反应后所得溶液的pH_______7。
用符号“>”“<”或“=”连接下列各项关系。
(1)第一电离能:Na_______________Mg,Mg_______________Ca。
(2)电负性:O_______________F,F_______________Cl。
(3)能量高低:ns_______________ (n+1)s,ns_______________np。
(4)主族序数_______________价电子数_______________元素最高正化合价
(8分)在某一周期,其零族元素的原子的外层电子构型为4s24p6,该周期中有A、B、C、D四种元素,已知它们的最外层电子数分别是2,2,1,7,且A、C元素的原子的次外层电
子数为8,B、D元素的原子的次外层电子数为18,则A、B、C、D分别为___________________,_____________,________________,_______________元素。
(6分)已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z,元素Y、X、Z的原子序数依次递增;②X在A、B、C、D中都不呈现它的最高化合价;③室温下单质A与某种常见一元强碱溶液反应,可得到B和C;④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是__________________________,Z是__________________________。
(2)写出③中反应的化学方程式:________________________________________________。
写出④中反应的化学方程式:___________________________________________________。
(10分)现有A、B、C三种元素,B原子序数大于A,A与B的质子数之和为27,质子数之差为5。9 g单质C与足量盐酸作用放出1.12 L氢气(标准状况),且生成C的三氯化物。回答下列
问题:
(1)A是_____________,B是_____________,C是_____________。
(2)三种元素的最高价氧化物对应水化物的酸碱性强弱顺序。