在下列物质中(填序号)
| A.Cl2 | B.NaI | C.H2S | D.CO2(E)CaCl2(F)N2 |
(G)CCl4 (H)Na2O (I)NH3 (J)HBr
(1)含离子键的物质是____________;
(2)含有共价键化合物的是_____________________;
(3)由 极性键形成的非极性分子是_______________;
极性键形成的非极性分子是_______________;
(4)由非极性键形成的非极性分子是_______________。
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlClx-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2↑。请回答下列问题:
(1)电池的负极材料为,发生的电极反应为。
(2)电池正极发生的电极反应为。
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是,反应的化学方程式为。
(4)组装该电池必须在无水、无氧的条件下进行,原因是。
某温度下向1L密闭容器中充入1mol N2和3 mol H2,使反应N2+3H2
2NH3达平衡,平衡混合气中N2、H2、NH3的浓度分别为M、N、G(mol/L).如果温度不变,只改变初始物质的加入量,要求M、N、G保持不变,则N2、H2、NH3的加入量用x、y、z表示时应满足的条件是:
①若x=0,y=0,则z=;
②若x="0.75" mol,则y=,z=;
③x、y、z取值必须满足的一般条件是(用含x、y、z方程表示,其中一个含x、z,另一
个含y、z)。
若将上述条件改为恒温、恒压,其它均不变,则
a.若x=0,y=0,则z=;
b.若x="0.75" mol,则y=,z=;
c.x、y、z取值必须满足的一般条件是。
随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。
(1)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A、CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0kJ/mol
B、CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-192.9kJ/mol
又知H2O(l)=H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式。
(2)下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。则c电极是(填“正极”或“负极”),
c电极上发生的电极反应式是。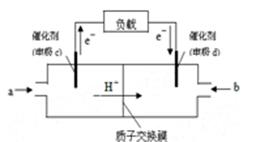
工程塑料ABS树脂(结构简式如下)合成时用了三种单体。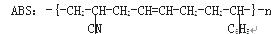
式中- C6H5是苯基。这三种单体的结构简式分别是:
、、
如图为以惰性电极进行电解的串联电解装置图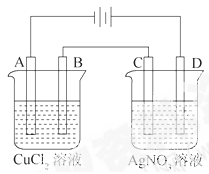
(1)写出A、B、C、D各电极上的电极方程式。
A;
B;
C’
D。
(2)在A、B、C、D各电极上析出生成物的物质的量比为。