下图中电极a、b分别为Ag电极和P t电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:
t电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:
(1)直流电源 中,M为 极。
中,M为 极。
(2)写出c极上发生的电极反应式 。
(3)Pt电极上生成的物质是 ,其质量为 g。
(4)AgNO3溶液的浓度(填增大、减小或不变。) , H2SO4溶液的浓度 。( 同上)
同上)
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为 g。
核电荷数小于18的两种元素A、B,A原子最外层电子数为a,次外层电子数为b;B原子M层电子数为(a-b),L层电子数为(a+b)。则A是___________元素,B是___________元素。
现有两种氧原子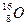 和
和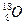 ,它们可分别形成16On和18Om两种气体单质。请完成下列问题:
,它们可分别形成16On和18Om两种气体单质。请完成下列问题:
(1)1 mol 16O中所含的中子数为__________个,1 mol 18O中所含的中子数为__________个。
(2)1 mol 16On中所含的中子数为____________mol,1 mol 18Om中所含的中子数为____________mol。
(3)若在同温、同压、同体积时,16On和18Om的中子数之比为6∶5,则n∶m=____________。
有若干克某金属,其各原子核内共有3.5×6.02×1023个中子,同质量的该金属和稀硫酸反应共有0.2 mol电子发生转移,生成6.02×1022个阳离子,这些阳离子共有3.0×6.02×1023个质子,则该金属摩尔质量为______________,原子核内有______________个质子,______________个中子,其核组成符号为______________。
锌的核电荷数为30,其最外电子层上只有2个电子,常显+2价。据此,请画出锌离子的结构示意图。
结构示意图为 的粒子。
的粒子。
x值可能为_________、_________、_________、_________、_________、_________,相应的粒子符号分别为_________、_________、_________、_________、_________、_________。