(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+ 转变为易吸收的Fe2+,,这说明维生素C具有 (填“氧化性”或“还原性”)
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应为:S+2KNO3 +3C=K2S+N2↑+3CO2↑.该反应中还原剂是 ,氧化剂是 。
+3C=K2S+N2↑+3CO2↑.该反应中还原剂是 ,氧化剂是 。
(14分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 |
OH-、Cl-、CO32-、NO3-、SO42- |
请根据以下实验事实逐步推出它们的名称并回答问题:
(1)
| 物质鉴定实验 |
推导结论 |
| ①用pH试纸测出A、B溶液呈碱性,C、D、E溶液呈酸性 |
A、B中含有的阴离子为________,C、D、E中含有的阳离子为________ |
| ②A溶液与E溶液反应既有气体又有沉淀产生;A与C反应只有气体产生 |
A为________,C含有的阳离子为________ |
| ③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀 |
D为________ |
(2)写出E溶液与过量的B溶液反应的离子方程式:_____________________________。
(3)在100 mL 0.1 mol/L的E溶液中,逐滴加入35 mL 2 mol/L NaOH溶液,最终得到沉淀的物质的量为__________________。
下图是中学常见物质间的转化关系。已知:
a.A为淡黄色固体,B为导致“温室效应”的主要物质;
b.E为常见金属,J为红褐色沉淀;
c.G在实验室中常用于检验B的存在;
d.L是一种重要的工业原料,常用于制造炸药,浓溶液若保存不当常呈黄色。
回答下列问题:
(1)A的电子式为;B分子属于分子(极性、非极性);
(2)反应①的化学方程式为,
反应②的离子方程式为,
(3)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为L。
(4)检验K中阳离子常用的方法是。
(5)L浓溶液的保存方法是。
在80 ℃时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4(g) 2NO2(g)ΔH >0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g)ΔH >0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)计算20~40 s内用N2O4表示的平均反应速率为____________mol· L-1·s-1。
(2)计算在80 ℃时该反应的平衡常数K=___________。
(3)反应进行至100 s后将反应混合物的温度降低,混合气体的颜色___________(填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有___________(填序号)。
| A.增大N2O4的起始浓度 | B.向混合气体中通入NO |
| C.使用高效催化剂 | D.升高温度 |
(5)如图是80 ℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60 ℃时N2O4物质的量的变化曲线。
(16分)
(1)1840年前后,瑞士科学家盖斯(Hess)指出,一个化学反应的热效应,仅与反应物的最初状态及生成物的最终状态有关,而与中间步骤无关,这就是著名的“盖斯定理”。现已知,在101 kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1和393.5 kJ·mol-1,则反应C(s)+2H2(g)= CH4(g)的反应热ΔH=__________,根据以上信息,你认为“盖斯定理”在我们确定一些化学反应的反应热时有何重要意义?__________。
(2)已知:2H2(g)+O2(g)====2H2O(g) ΔH1
2H2(g)+O2(g) ====2H2O(l)ΔH2
2CO(g)+O2(g)====2CO2(g)ΔH3
①写出液态水转化为气态水的热化学方程式:___________________________________。
②CO和H2分别燃烧生成CO2(g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是__________。
(14分)某化学反应2A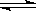 B+D在四种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表: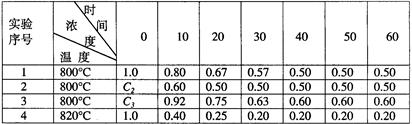
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率V(B)为mol/(L·min)。
(2)在实验2,A的初始浓度C2=mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3V1(填>、=、<),且C31.0mol/L(填>、=、<)
(4)比较实验4和实验1,可推测该反应是反应(选填吸热、放热)。