下列叙述不正确的是
| A.H2S、H2O、HF的稳定性依次增强 | B.Na+、Mg2+、Al3+的氧化性依次减弱 |
| C.H4SiO4、H2CO3、H2SO4的酸性依次增强 | D.KOH、NaOH、Mg(OH)2的碱性依次减弱 |
用惰性电极实现电解,下列说法正确的是
| A.电解氢氧化钠稀溶液,溶液浓度增大,pH变小 |
| B.电解氯化钠溶液,溶液浓度减小,pH不变 |
| C.电解硝酸银溶液,要消耗OH-,溶液pH变小 |
| D.电解稀硫酸,实质是电解水,溶液pH不变 |
某电解池内盛有CuSO4溶液,插入两根电极,接通直流电源后,欲达到如下要求:①阳极质量不变 ②阴极质量增加 ③电解液pH减小,则应选用的电极是
| A.阴、阳两极都用石墨棒 | B.铜作阳极,铁作阴极 |
| C.铁作阳极,铜作阴极 | D.铜作阳极,铂作阴极 |
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.电解后溶液中c(H+)为2 mol/L |
| B.上述电解过程中共转移2 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol |
| D.原混合溶液中c(K+)为2 mol/L |
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为CoO2+LiC6 LiCoO2+C6,下列说法正确的是
LiCoO2+C6,下列说法正确的是
| A.充电时,电池的阴极反应为LiC6-e-===Li++C6 |
| B.放电时,电池的正极反应为CoO2+Li++e-===LiCoO2 |
| C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质 |
| D.锂离子电池的比能量(单位质量释放的能量)低 |
电浮选凝聚法是工业上采用的一种污水处理方法:在污水中通电生成Fe(OH)3胶体,Fe(OH)3胶体可吸附污染物而沉积下来,具有凝聚净化的作用:电极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去浮渣层,即起到了浮选净化的作用。某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法不正确的是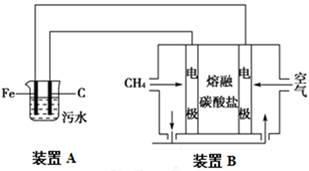
| A.装置A中铁片为阳极,发生的电极反应是Fe-2e- = Fe2+ |
| B.装置B中通入空气的电极反应是O2+2CO2+4e- = 2CO32— |
| C.污水中加入适量的硫酸钠,可增强溶液的导电性,提高污水的处理效果 |
| D.标准状况下,若A装置中产生了44.8L气体,则理论上B装置中要消耗CH4为1.12L |