 是周期表中原子序数依次增大的前20号元素。
是周期表中原子序数依次增大的前20号元素。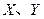 同周期。
同周期。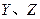 同主族,Zn-与
同主族,Zn-与 离子的电子层结构相同。由这四种元素形成的单质、化合物有如下图转化关系。已知:常温下
离子的电子层结构相同。由这四种元素形成的单质、化合物有如下图转化关系。已知:常温下 为液体,
为液体, 为气态化合物,且
为气态化合物,且 均为直线型分子;
均为直线型分子; 是由元素
是由元素 形成的常见化合物。
形成的常见化合物。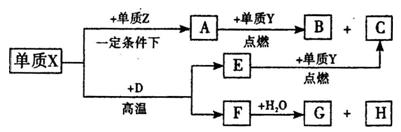
(1)元素 的名称 ,
的名称 , 的电子式 ,F晶体中含有的化学键类型 。
的电子式 ,F晶体中含有的化学键类型 。
(2)写出 的化学式:
的化学式: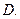 、
、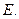 。
。
(3)①已知38g 与单质
与单质 完全反应生成
完全反应生成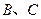 时放出
时放出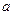 kJ的热量,写出该反应的热化学方程式:
kJ的热量,写出该反应的热化学方程式:
②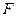 与水反应的化学方程式:
与水反应的化学方程式:
下表是元素周期表的一部分,回答下列有关问题:(用元素符号或化学式填空)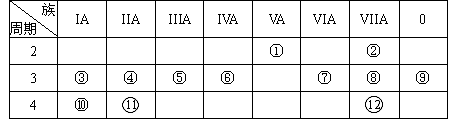
(1)写出下列元素符号:①________,⑥________,⑦________。
(2)画出原子的结构示意图:④________,⑤________,⑧________。
(3)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是________,最不活泼的元素是________。
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是________,碱性最强的是________,呈两性的氢氧化物是________。
(5)在③与④中,化学性质较活泼的是________,怎样用化学实验证明:答:________
在⑧与⑿中,化学性质较活泼的是________,怎样用化学实验证明?答:____________。(用化学反应方程式表示)
(每空1分,共12分)
(1)浓硫酸与木炭粉在加热条件下的化学方程式为____________。
(2)已知酸性KMnO4溶液可以吸收SO2,试用图4-6所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号): __________→__________→__________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是________,B瓶溶液的作用是_________,C瓶溶液的作用是_________________________。
(4)装置②中所加的固体药品是_______________,可确证的产物是_______。
(5)装置③中所盛溶液是__________,可验证的产物是__________。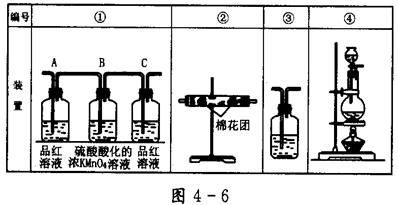
(每空1分,共9分)A、B、C、D四种元素的最高正价依次为1、4、5、7,其核电荷数按B、C、D、A的次序增大;已知B原子的次外层电子数为2,C、D、A原子的次外层电子数均为8;A原子核外电子总数不超过20。试回答:
(1)各元素符号为:A_____B_____C_____D_____
(2)写出B、D最高价氧化物对应水化物的分子式: ___、____,并比较其酸性强弱:_________
(3)写出分子BD4的电子式:
(4)用电子式表示AD的形成过程:
(每空1分,共6分)根据下列变化进行推断。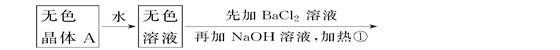 \x(气体B,遇HCl冒白烟白色沉淀C
\x(气体B,遇HCl冒白烟白色沉淀C
且已知强热A产生的气态物质的平均式量(平均相对分子质量)为26.3。
(1)推断A、B、C、D的化学式:A________,B________,C________,D________。
(2)写出①②变化的离子方程式:
①____________________________________________________;
②_____________________________________________________。
(最后一空2分,其余每空1分,共8分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
 (1)图中A、C分别表示、,E的大小对该反应的反应热有无影响?。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,理由
(1)图中A、C分别表示、,E的大小对该反应的反应热有无影响?。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,理由
是; (2)图中△H=KJ·mol-1;
(2)图中△H=KJ·mol-1; (3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求
计算过程)。