原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16,单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答: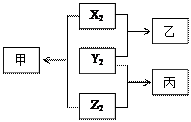
(1)Y2的电子式是___ ______;该分子中有 个σ键, 个π键。
(2)甲属于(填“极性”或“非极性”) 分子;晶体中甲分子的配位数为  。
。
(3)乙分子的VSEPR模型名称为 ,分子的立体构型名称为 。
(4)写出乙与Z2反应生成丙的化学方程式 。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式: ,氧化剂为 。
氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子(指H+)形成的,类似于NH4+,因此有类似于 NH4+的性质。
⑴、写出N2H62+在足量碱性溶液中反应的离子方程式
。
⑵、NH2-的电子式为。
⑶、N3-有个电子。
⑷、写出二种由多个原子组成的含有与N3-电子数相同的物 质的化学式。
质的化学式。
⑸、等电子数的微粒往往具有相似的结构,试预测N3—的构型。
⑹、据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是。
D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,他们的最简单氢化物分子的空间结构依次是正四面体、三角锥形、正四面体、V形、直线型。请回答下列问题:
(1)、写出工业制E的氢化物的化学方程式
(2)、Z在元素周期表中位于族,Z的单质与强碱溶液反应的离子方程式
(3)、试比较D和X的最高价氧化物熔点的高低并说明理由
(4)、写出Y的氧化物的化学式、
按要求完成下列各小题
(1)、写出钙的核外电子排布式
(2)、画出氟的价电子轨道表示式
(3)、写出含有一个手性碳原子的分子
(4)、写出甲烷中σ 键的具体类型(即参与成键的原子轨道)
键的具体类型(即参与成键的原子轨道)
写出下列反应的离子方程式
(1) 用稀硫酸清除铁锈(Fe2O3)
(2) 在澄清石灰水中滴加碳酸钠溶液
(3) FeCl3溶液中加入NaOH溶液:
(4) 铁跟稀硫酸反应:
(5) 少量CO2通入澄清石灰水中:
(2分)写出符合离子方程式Ba2++SO42-=BaSO4↓的一种化学方程式