某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素碳与硅的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红色试纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。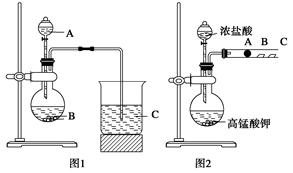
根据图1回答:
(1)写出选用物质的名称:A________ ____,B_____ _____ ,C____________;
(2)烧瓶中反应的离子方程式为_______________________________________________
烧杯中反应的离子方程式为_______________________________________________。
根据图2回答:
(3)乙同学的实验原理是______________________________________________ _
(4)B处的实验现象是______________________________________________ _;
(5)B处的反应的离子方程式: ___________________________________________ _ 。
实验室利用右图装置进行中和热的测定,请回答下列问题: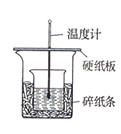
(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用次,
某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别
测量酸和碱的温度,你是否同意该同学的观点,为什么?
(3)请为本实验设计数据记录表格:
某校化学研究性小组,利用下列提供的实验装置和试剂对某种燃煤所含元素进行定性和定量检测,试回答: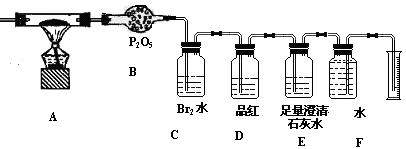
(1)将燃煤充分燃烧,产生气体经化学分析主要含有CO2、H2O、SO2、N2四种气体
(2)称取该燃煤样品Wg,通入纯氧使其充分燃烧,检测该燃煤中所含上述元素的质量分数。利用下列装置进行实验:
①指出上述装置中D、E的作用
D, E
为了测得相应数据,进行如下操作(忽略CO2在C、D中的溶解)
a.实验前用托盘天平称得B、C、D、E的质量分别为W1、W2、W3、W4
b.实验完成后称得B、C、D、E的质量分别为m1、m2、m3、m4
c.通过正确实验操作,用F装置测得收集气体体积为V L
②为了准确测量F中收集到的气体体积,正确的实验操作是
③测定燃煤中的硫的质量分数,当观察到溴水不完全褪色,品红不褪色时,燃煤中含硫元素的质量分数的表达式为。当观察到
现象时,无法测定燃煤中硫元素的质量分数。
1)在实验室中用MnO2和浓盐酸反应制备氯气,其反应的化学方程式为_______________;
(2)某同学欲制取2.24L(标况)氯气,其做法是称取8.7g二氧化锰与40mL10mol·L—1的浓盐酸反应,其做法能否达到目的 _______________(填“能”、“或“不能”)。通过计算和文字叙述说明之。
25.课本“交流•研讨”栏目有这样一组数据:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收249kJ的能量;形成水分子中1 molH—O键能够释放463kJ能量。
下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在下边的横线上。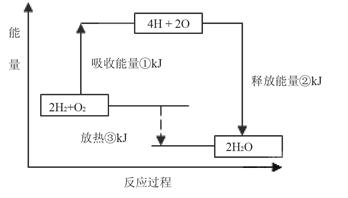
①____________kJ②____________kJ③____________kJ
根据下图转化回答有关问题:
(1)①写出AC反应生成乙酸乙酯的化学方程式_______________;
反应类型_______________;
②B的结构简式为_______________。
(2)某同学在实验室用如图所示的装置来制取乙酸乙酯。请回答下列问题:
①浓硫酸的作用是______________________________。
②饱和碳酸钠溶液的主要作用_______________。
③装置中通蒸气的导管只能插到饱和碳酸钠溶液的液面处,不能插入溶液中,目的_______________ ,长导管的作用是_______________。
④若要把制得的乙酸乙酯分离出来,应采用的实验操作是_______________。
⑤进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是_______________。
⑥生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述不能说明该反应已达到化学平衡状态的是(填序号) _______________ 。
| A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水 |
| B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸 |
| C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸 |
| D.正反应的速率与逆反应的速率相等 |
E.混合物中各物质的浓度不再变化