(14分)
实验室用下图所示装置制备溴苯,并验证该反应是取代反应。
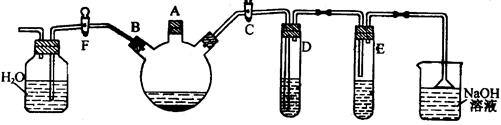
(1) 关闭F活塞,打开C活塞,在装有少量苯的三颈瓶中由A口加入少量溴,再加入少量铁屑,塞住A口,则三颈瓶中发生反应的化学方程式为: 。
(2) D试管内装的是 ,其作用是 。
(3) E试管内装的是 ,E试管内出现的现象为 。
(4) 待三口烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,可以看到的现象是 。
(5) 上一步得到粗溴苯后,要用如下操作精制:a蒸馏; b水洗; c用干燥剂干燥; d 10%NaOH溶液洗涤; e水洗,正确的操作顺序是 。
Ⅰ.已知测定中和热的实验步骤如下:①量取50mL 0.25 mol/L硫酸倒入小烧杯中,测量温度②量取50mL 0.55mol/L NaOH溶液,测量温度;③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)NaOH溶液稍过量的原因。
(2)加入NaOH溶液的正确操作是 (填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是。
(4)设溶液的密度均为1g·cm-3,中和后溶液的比热容c="4.18" J·(g·℃)-1,请根据实验数据求出中和热为 写出该反应的热化学方程式_________
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量(填“小于”、“等于”或“大于”)57.3 kJ,原因是
Ⅱ.某烧碱样品含有少量不与酸作用的杂质,为了测定其纯度,进行以下操作:
A.在250 mL的容量瓶中定容配成250 mL烧碱溶液
B.用碱式滴定管量取25.00 mL烧碱溶液于锥形瓶中,并滴入几滴酚酞作指示剂
C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解
D.将物质的量浓度为M的标准硫酸溶液装入润洗好的酸式滴定管中,调节液面使开始读数为V1 mL
E.在锥形瓶下垫一张白纸,滴定至溶液恰好由红色变为无色时,记下读数为V2 mL
试填空:
(1)正确操作步骤的顺序是(用字母表示)。
(2)观察滴定管液面的高度时应注意
(3)E步骤的操作中锥形瓶下垫一张白纸的作用是。
(4)某学生实验时把锥形瓶用烧碱样品溶液洗涤,使测定的浓度_________(填“偏高”“偏低”或“无影响”),原因是
(5)该烧碱样品纯度的计算式为_________________________。
实验室有一瓶Na2SO3固体,可能含有NaCl、Na2SO4、BaCl2、K2CO3、K2SO4中的一种或几种杂质,通过下列实验确定该样品的成分及Na2SO3的质量分数。请回答下列问题:
已知:
①取少量样品于试管中,加水振荡,未见沉淀生成:
②通过元素分析仪器的检测,得知该样品中不含K元素;
③用下图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
(1)按气流从左到右方向,正确的连接顺序为:A接____,接,接B。
(2)利用所组装置,由分液漏斗向烧瓶中滴加l0mL水,理论上将排入量筒中mL液体。
(3)液体X是,其作用是。
(4)Y的作用是防止产生的气体溶于水,下列历给试剂符合要求的是____(填序号)。
A.甲苯 B.四氯化碳 C.酒精 D.浓硫酸
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(已折算成标准下的状况)。根据此信息,回答以下问题:
(5)对实验获得准确的气体体积无益的操作有(填序号)
①检查装置的气密性:
②实验结束后,将连通ZJ、丁的导管中的水也引入量筒;
③读数时视线与量筒内凹液面最低相切点水平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出。
(6)向充分逸出气体后的溶液中加入过量BaCl2溶液,得到白色沉淀13.98g。根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是,含有的杂质是。
为研究温度对Cl2与KOH反应的影响,设计实验如下:
在蒸馏烧瓶中装入足量MnO2,分液漏斗中装足量浓盐酸,大试管A中装4mol/LKOH溶液15mL,并置于75℃水浴中,大试管B中装02mol/LKOH溶液,并置于冰水中,C中装NaOH溶液。
试回答下列问题:
(1)水浴加热有什么优点?
(2)如何判断A中已经反应完全?
(3)分离A中生成的两种盐,检测发现其中KCl为005mol(不考虑HCl挥发),写出A中发生的化学方程式
(4)分离B中生成的两种盐, 其物质的量之比为1:1,写出离子方程式。
其物质的量之比为1:1,写出离子方程式。
(5)试管B要置于冰水中降温的主要原因是:
| A.从试管A中出来的气体温度较高,易使试管B中的溶液温度升高 | |
| B.防止生成的盐分解 | C.催化剂在冷水中活性最强 |
| D.该反应是放热反应,为防止温度过高,采用降温 |
(6)图一中,分液漏斗下端连接玻璃管并伸入液面下,其作用是什么? 可以用图二代替吗?。
可以用图二代替吗?。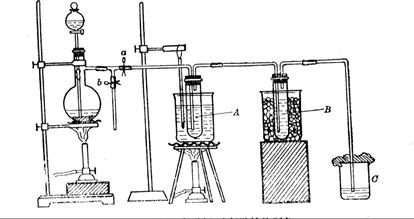
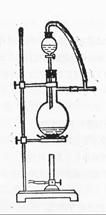
图一图二
Fe(OH)2由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用右图装置使用Fe,H2SO4(稀),NaOH溶液可在还原性气氛中制取Fe(OH)2白色沉淀,且较长时间内不变色,其中C为弹簧夹。(提示:还原性气氛如氢气环境)
(1)则锥形瓶A中应加入的药品为_________________.
(2)锥形瓶B中应加入的药品为__________________.
(3)容器A中的反应开始后,请简单写出完成制备Fe(OH)2的后续操作步骤。
①_____________________②_______________________________。
(4)若在反应开始之前先关闭弹簧夹C,则实验现象为:
;
请写出此时B瓶中发生的化学反应的离子方程式:
;
喷泉实验是一个有趣实验。现有250mL的烧瓶充满某种气体进行实验。设玻璃导管长35cm,胶 头滴管中可挤出0.50mL水。(不考虑溶质的损失)
头滴管中可挤出0.50mL水。(不考虑溶质的损失)
(1)0.5mL水中至少要溶解毫升该气体(标准状况),水才能从尖嘴管喷出(假设水面保持不变)?
(2)下列气体能做成喷泉实验的是____。(少选、错选不计分)
| 气体 |
A |
B |
C |
D |
E |
| 溶解度(标况) |
2.6 |
40 |
5.8 |
10.2 |
23.1 |
(3)假设NO2能进行喷泉实验,实验后该烧瓶中溶液的物质的量浓度为多少?(保留两位有效数字)