下列说法正确的是
| A.SiH4比CH4稳定 |
| B.O2-半径比F-的小 |
| C.Na与Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D.P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱 |
向50 mL 18 mol·L-1 H2SO4溶液中加入足量的Cu片并加热,充分反应后,被还原的H2SO4的物质的量为()
| A.小于0.45 mol |
| B.等于0.45 mol |
| C.在0.45~0.90 mol之间 |
| D.大于0.90 mol |
下列叙述正确的是()
| A.失电子越多的还原剂,其还原性越强 |
| B.阴离子只能失去电子被氧化,作还原剂 |
| C.含有最高价元素的化合物不一定具有强氧化性 |
| D.最外层电子数较少的金属元素,一定比最外层电子数多的金属元素活泼性强 |
工业上从含硒的废料中提取硒的方法之一是用硫酸和硝酸钠处理废料,获得亚硝酸和少量硒酸,再与盐酸共热,硒酸被转化为亚硒酸:2HCl+H2SeO4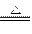 H2SeO3+Cl2↑+H2O,通SO2于亚硒酸溶液中,单质硒即析出。据此,下列叙述正确的是()
H2SeO3+Cl2↑+H2O,通SO2于亚硒酸溶液中,单质硒即析出。据此,下列叙述正确的是()
| A.H2SeO4氧化性强于Cl2 |
| B.亚硒酸氧化性强于H2SO3 |
| C.二氧化硒的还原性强于二氧化硫 |
| D.析出1 mol Se需H2SeO3,SO2,H2O各1 mol |
用0.1 mol·L-1的Na2SO3溶液30 mL恰好将2×10-3 mol的 还原,则元素X在还原产物中的化合价是()
还原,则元素X在还原产物中的化合价是()
| A.+1 | B.+2 | C.+3 | D.+4 |
人体内的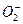 对健康有害,能使人过早衰老,这是因为
对健康有害,能使人过早衰老,这是因为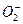 在人体内释放出氧化性极强的活性氧的缘故,医学上试图用对人体无害的亚硒酸钠清除人体内的活性氧,这是利用了亚硒酸钠的()
在人体内释放出氧化性极强的活性氧的缘故,医学上试图用对人体无害的亚硒酸钠清除人体内的活性氧,这是利用了亚硒酸钠的()
| A.还原性 |
| B.氧化性 |
| C.催化性 |
| D.既有氧化性,又有还原性 |