一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,总反应式为:2C2H6+7O2+8KOH ==4K2CO3+10H2O,下列推断正确的是
| A.负极反应为7O2+14 H2O+28e— →28OH— | |
B.每消耗1molC2H6,则电路上转移的电子为14 mol |
C.放电一段时间后,负极周围的pH升高 |
| D.放电过程中KOH的物质的量浓度不变 |
NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol CO2中含有原子数NA |
| B.1 L 1mol/L的硫酸钠溶液中,所含Na+数为NA |
| C.标准状况下,11.2 L水所含分子数为0.5 NA |
| D.1 mol Fe含有原子数NA |
300 mL 0.2 mol/L KCl溶液与100 mL 0.3 mol/L AlCl3溶液中Cl-物质的量浓度之比是
| A.1∶3 | B.2∶3 | C.2∶1 | D.2∶9 |
在盛放酒精的试剂瓶的标签上应印有的警示标志是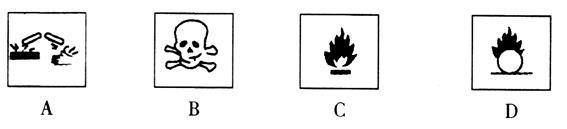
将5 mol/L盐酸10 mL稀释到200 mL,再取出5 mL,这5 mL溶液的物质的量浓度是
| A.0.05 mol/L | B.0.25 mol/L | C.0.1 mol/L | D.0.5 mol/L |
下列说法中正确的是
| A.标准状况下,22.4 L水中所含的分子数约为6.02×1023个 |
| B.1 mol Cl2中含有的原子数为NA |
C.标准状况下,a L氧气和氮气的混合物含有的分子数约为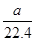 ×6.02×1023个 ×6.02×1023个 |
| D.从1 L0.5 mol·L-1NaCl溶液中取出100 mL,剩余溶液中NaCl物质的量浓度为0.45 mol·L-1 |