键能是破坏1mol化学键吸收的热量或者生成1mol化学键放出的热量,解释下列物质性质的变化规律与物质结构间的因果关系时,与键能无关的变化规律是
①HF、HCl、HBr、HI的热稳定性依次减弱 ②NH3易液化 ③F2、C12、Br2、I2的熔、沸点逐渐升高 ④H2S的熔沸点小于H2O的熔沸点
③F2、C12、Br2、I2的熔、沸点逐渐升高 ④H2S的熔沸点小于H2O的熔沸点 ⑤NaF、NaCl、NaBr、NaI的熔点依次减低
⑤NaF、NaCl、NaBr、NaI的熔点依次减低
| A.②③④ | B.③④⑤ | C.②③④⑤ | D.全部 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) + 3H2(g) 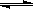 2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
平衡时反应中的能量变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量a kJ |
| ② |
2 |
3 |
0 |
放出热量b kJ |
| ③ |
2 |
6 |
0 |
放出热量c kJ |
下列叙述正确的是 ( )
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
T ℃时,在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论不正确的是( )
A.容器中发生的反应可表示为:3X(g)+Y(g) 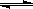 2Z(g) 2Z(g) |
| B.反应进行的前3 min内,用X表示的反应速率 v(X)=0.3mol/(L·min) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件可能是使用了催化剂 |
反应2A(g)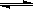 2B(g)+C(g)(正反应为吸热反应),达到平衡时,要使逆反应速率降低,A的浓度增大,应采取的措施是 ( )
2B(g)+C(g)(正反应为吸热反应),达到平衡时,要使逆反应速率降低,A的浓度增大,应采取的措施是 ( )
| A.减压 | B.降温 | C.加压 | D.增大B的浓度 |
下列各组试剂不需要任何其他试剂就可以区分开的是()
| A.NaCl、AgNO3、NH4Cl、Na2SO4 | B.NaHCO3、H2SO4、KNO3、KOH |
| C.CuSO4、NaCl 、KOH、BaCl2 | D.KNO3、HCl、NaOH、K2CO3 |
下列物质中属于非电解质的是()
| A.CO2 | B.NaOH | C.H2SO4 | D.Fe |