在密闭容器中进行如下反应:H2(g) +I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是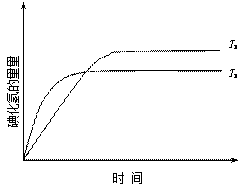
| A.T1>T2,ΔH>0 | B.T1>T2,ΔH<0 |
| C.T1<T2,ΔH>0 | D.T1<T2,ΔH<0 |
在2 L密闭容器中,发生3A(g)+B(g)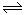 2C(g)的反应,若最初加入A和B都是4 mol,A的平均反应速率为0.12 mol·L-1·s-1,则10 s后容器中B的物质的量浓度是()
2C(g)的反应,若最初加入A和B都是4 mol,A的平均反应速率为0.12 mol·L-1·s-1,则10 s后容器中B的物质的量浓度是()
| A.1.4 mol·L-1 | B.1.6 mol·L-1 |
| C.1.8 mol·L-1 | D.3.2 mol·L-1 |
下列叙述正确的是()
| A.液晶是由分子较大、分子形状呈长形或碟形的物质形成的晶体 |
| B.制造光导纤维的主要材料是高纯度硅,属于原子晶体 |
| C.H2O分子比H2S分子稳定是因为水分子之间存在氢键 |
| D.NaCl和MgO晶体熔融时克服的作用力相同 |
一定温度下的反应A(g)+3B(g) 2C(g),下列叙述不能表明它达到化学平衡的是
2C(g),下列叙述不能表明它达到化学平衡的是
A.C的生成速率与C的分解速率相等
B.混合气体的总物质的量不再变化
C.A、B、C的浓度不再变化
D.单位时间内生成a mol A,同时生成3amol B
下列各组顺序的排列不正确的是()
| A.离子半径:Na+>Al3+>F- |
| B.热稳定性:HCl>PH3>AsH3 |
| C.酸性:H3PO4>H2CO3>H2SiO3 |
| D.熔点:CH3(CH2)3CH3>(CH3)2CHCH2CH3>CH3C(CH3)3 |
已知空气-锌电池的电极反应为:锌片:2Zn+4OH--4e-=2ZnO+2H2O;碳棒:O2+2H2O+4e-=4OH-,据此判断,锌片是()
| A.正极,被还原 | B.正极,被氧化 |
| C.负极,被还原 | D.负极,被氧化 |