为测定某卤代烃的组成, 某同学设计实验如下:①量取该卤代烃液体11.4mL, 加入适量NaOH溶液, 加热反应至液体不分层;②冷却后用稀硝酸酸化, 再加入过量硝酸银;③过滤沉淀, 洗涤沉淀2~3次;④将沉淀干燥后称重。
回答下列问题:
(1)①中加入NaOH的目的是____________________________________________________
(2)②中加入过量硝酸银的目的是______________________________________________
(3)若②中生成的沉淀为淡黄色, 则该卤代烃中的卤原子是________
(4)若称得沉淀的质量为37.6g, 又测得卤代烃的密度为1.65g·mL-1, 其蒸气密度是相同条件下氢气密度的94倍。则该卤代烃分子中含有________个卤原子。
(5)写出该卤代烃可能的结构简式和名称:______________ ___
(本题共12分)用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
36、在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发、_________、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________。
a. 蒸发的目的是得到热饱和溶液
b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液
d. 应蒸发至有较多晶体析出时为止
37、由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________。
a. 得到热饱和溶液b. 析出晶体
38、若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:___________________;用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_______________________________________________________________。
39、该流程产生的物质中,除Ca2+能被海洋生物利用外,还需综合利用的物质是_________。
40、MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和水,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a:b≈______________(取整数值)。
(本题共11分)本题有2小题。在一体积为2L的密闭容器中,气态物质A、B、E的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度A的转化率增大。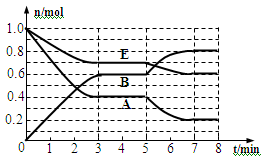
29、写出此反应的化学方程式_________________________________;此反应是___________热反应。
30、根据图数据,从反应开始到第一次达到平衡时平均速率v (E)为________________。
31、在5~7 min内曲线变化的原因可能是____(填编号)
A. 降低了温度 B. 使用了催化剂
C. 减小了容器的体积 D. 减少了A的物质的量
32、设该反应达到平衡时的平衡常数为K1,保持温度不变,将容器体积减少一半,达到新的平衡后,测得B的平衡浓度为原来的2.2倍,平衡常数为K2,则_______(填编号)
A. 平衡向正反应方向移动,且K2 > K1
B. 平衡移动过程中,正反应速率大于逆反应速率
C. 达到新平衡时,A的浓度增大,且K1 > K2
D. 达到新平衡时,E的浓度是原来的2倍多,且K1 = K2
已知在25℃时,亚硝酸、次氯酸和氢硫酸的电离常数分别为:
亚硝酸 Ki = 4.6×10-4
次氯酸 Ki = 3.0×10-8
氢硫酸 Ki 1= 9.1×10-8Ki 2 = 1.1×10-12
33、写出氢硫酸的第一级电离平衡常数表达式:Ki1 = _________________。
34、在相同条件下,试比较H2S、HS-、HClO和HNO2的酸性强弱:______>______>_____>_______。
35、保持温度不变,在氢硫酸溶液中加入少量盐酸,下列量会变小的是_____(填序号)
A.c(S2-)
B.c(H+)
C.Kw
D.氢硫酸电离平衡常数
E.氢硫酸的电离度
(本题共13分)A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E顺序增大;C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A和气体物质EB4;EB4蒸气的密度是相同条件下空气密度的3.586倍。
23、指出A在元素周期表中的位置_________。
24、写出D2A2的电子式__________;写出CB与EA2反应的化学方程式___________________。
25、下表是不同物质中的键长和键能的数据,其中a、b、d未知,通过表中的数据分析,估计出a、b、c、d的大小顺序为______________________________。
| 共价键 |
C-C |
C=C |
 C C C C |
C-O |
C=O |
H-F |
N=N |
 N N N N |
| 键长(nm) |
0.154 |
0.134 |
0.120 |
0.143 |
0.122 |
0.092 |
0.120 |
0.110 |
| 键能(kJ/mol) |
a |
b |
358 |
c=805 |
569 |
d |
氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。
26、不能通过电解纯净的液态HF获得F2,其原因是_________;但电解液态KHF2时,两极分别得到F2和H2,则F2在电解池的_____极产生。
27、利用化学反应也能制取氟。请配平下列化学方程式:
____K2MnF6+____SbF5→____KSbF6+____MnF3+____F2↑
28、一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量f随pH的分布曲线如图示。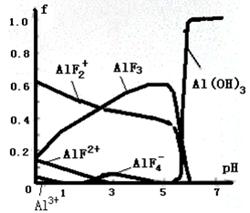
用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式:____________________。
(12分)从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。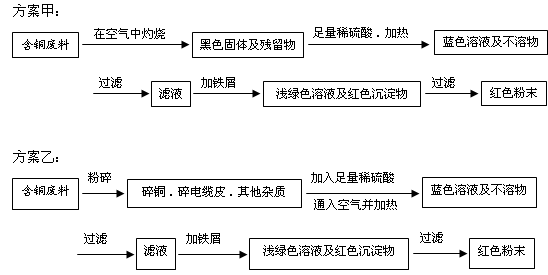
(1)两个方案中,符合当前生产中绿色化学理念的是方案。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
①先取a g的晶体进行脱水实验,获得无水固体为(a-1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00 mol·L-1的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。通过计算测知该晶体的化学式是。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3 =" 2" CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+ = Fe 3+ + Ce3+
计算上述样品中CuCl的质量分数。(写出计算过程)
(1)某课外活动小组同学用下图装置进行实验
试回答下列问题:
①若开始时开关K与a连接,则铁发生电化学腐蚀中的腐蚀。
②若开始时开关K与b连接,则总反应的离子方程式为。
(2)芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如下图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为。此时通过阴离子交换膜的离子数(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钠溶液从出口(填“A”、“B”、“C”或“D”)导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因:。
④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为,已知H2的燃烧热为285.8 kJ·mol-1,则该燃料电池工作产生36 g H2O时,理论上有kJ的能量转化为电能。