某学校化学课外活动小组的同学,取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
| 测定时刻 |
5:05 |
5:10 |
5:15 |
5:20. |
5:25 |
5:30 |
| pH |
4.95 |
4.94 |
4.94 |
4.88 |
4.86 |
4.85 |
(1)所降雨水 _________(填“是”或“不是”)酸雨,在测定的时间内雨水的酸性____________(填“增强”或“减弱”)。
(2)经调查,这一地区有一个硫酸厂(生产过程中产生硫的氧化物)和一个电镀厂,这些工厂使用的燃料主要是煤(煤中含有硫元素)。另外,这一地区的生活燃料主要也是煤,还有液化石油气。试分析造成这一地区酸雨的主要原因是什么? 你认为应采取什么措施?
利用玻璃瓶和一些必要的药品进行如下实验,观察实验现象,并把观察到的现象填在空白处。
| 实验内容 |
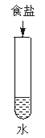 |
 |
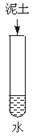 |
 |
| 振荡 |
||||
| 静置 |
图10是实验室制取气体的一些装置,据图回答有关问题。(提示:以下所选装置均填装置标号)
(1)写出序号为①②③的仪器名称:① ;② ;③。
(2)写出你知道的化学实验中可选用装置C制取气体的药品是 ;
①该装置中试管口要略向下倾斜目的是 ;
②收集所得气体可选用的一种装置是 。
(3) 某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5;
②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;
③将带火星的木条依次插入1~5号瓶中,把观察到现象和计算数据,填入下表。
| 集气瓶标号 |
1 |
2 |
3 |
4 |
5 |
| 集气瓶中氧气的体积分数 |
28.9% |
36.8% |
44.7% |
52.6% |
60.5% |
| 带火星木条的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
试回答下列问题:
①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,可采用的发生装置是(填标号)。
②根据以上实验事实,下列说法中正确的是(填写相应的标号)。
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈。
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。你认为上图中最适合制取乙炔气体的发生装置是 ;如果用图11所示装置收集乙炔,
气体应从 (填“a”或“b”)端管口通入。
小东同学用如图9所示气密性良好的装置进行有关实验。
图9中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,其左端密封有空气和足量白磷和红磷(提示:物质燃烧所需温度必须达到该物质的着火点,白磷着火点40 ℃,红磷的着火点240 ℃),右端跟空气相通,实验开始前,活塞处在5 cm处。
(1)实验开始时,可以观察到玻璃管内白磷,红磷。实验结束后,恢复至常温,活塞应停在约cm处,据此可得出关于空气组成的结论是。
(2)根据以上实验可以推测:白磷的物理性质和化学性质(各写一点)。
某校研究性学习小组对汉江某段水质的状况进行相关的调查研究。
(1)图8所示的自制净水器中的物质,可除去水中的异味和色素。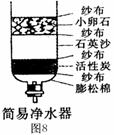
(2)硬水会给生活和生产带来许多麻烦,长期饮用硬水可能会引起体内结石,如用硬水洗涤衣物,既浪费肥皂又洗不干净,时间长了还会使衣物变硬。通过化学学习,我们知道可用来区分该水属于硬水还是软水;生活中要降低水的硬度,可采用的方法是。
(3)你认为下列行为会造成内河水质下降的是。(填标号)
A.在河边种植花草树木 B.居民将生活污水直接排入内河C.将垃圾倒入内河中
在“氧气的制取和性质”实验中,某同学取一段纱窗网上还能任意弯曲的细铁丝,在新制的氧气中做“铁丝燃烧”的实验。结果没有观察到“火星四射”的现象,请分析此实验失败的可能原因:(写一种);经过改进后实验成功了,其反应的文字表达式。实验时要在集气瓶底部铺一层细沙或装少量水的原因是。